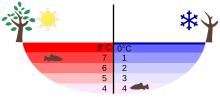
Anomalie de densitate
Pentru majoritatea substanțelor ia densitatea cu scăderea temperaturii până la o schimbare a stării de timp. O substanță chimică prezintă o anomalie a densității atunci când densitatea acesteia scade sub o anumită temperatură atunci când temperatura scade, adică substanța se extinde când se răcește (expansiune termică negativă).
Anomalii de densitate apar în elementele chimice stibiu , bismut , galiu , germaniu , topit litiu , plutoniu , siliciu și telur , de asemenea , în aliaje , cum ar fi din metal Wood și compuși , cum ar fi zirconiu tungstatul ( ) , sau cianură de zinc . Apa este cea mai importantă substanță în care apare o astfel de anomalie : pe de o parte, se atinge densitatea maximă a apei lichide peste 0 ° C, pe de altă parte, gheața are o densitate mai mică decât apa lichidă.
Unele gaze lichefiate puternic polare prezintă, de asemenea , anomalii de densitate, de ex. B. fluorură de hidrogen și amoniac . Chiar dacă β-staniu este transformat într-o altă modificare (α-staniu) sub 13,2 ° C , densitatea sa se schimbă, dar aici este ireversibilă.
utilizare
Substanțele cu densitate anormală pot fi utilizate în inginerie ca compensator al dilatării termice. Procedând astfel, substanțele cu dilatare termică pozitivă și substanțele cu dilatare termică negativă (adică cu anomalii de densitate) sunt reunite, astfel încât atunci când se schimbă temperatura, dilatarea și contracția sunt echilibrate și materialul nu își modifică deloc volumul sau se modifică într-un mod precis definit cu temperatura . Expansiunea termică aproape de zero garantează performanțe neschimbate la diferite temperaturi.
Un exemplu bun din viața de zi cu zi pentru materiale cu o dilatare termică aproape de zero sunt vitroceramica - plite de acest fel. B. Ceran . Acestea au o rezistență ridicată la schimbările de temperatură , astfel încât sticla să nu crape dacă este încălzită pe o parte în timp ce cealaltă parte este la temperatura camerei . Acest lucru se datorează faptului că unele faze conținute în aceste ceramice au o anomalie în densitate. Sticla ceramică este reglată cu ajutorul compoziției chimice în așa fel încât expansiunea termică negativă a acestor faze compensează expansiunea termică pozitivă a altor faze atunci când temperatura se schimbă. Apoi, întreaga plită nu prezintă nicio expansiune termică, iar Ceranul nu se sparge dacă nu este încălzit uniform peste tot.
Mai ales în ingineria z. B. în fabricarea instrumentelor de precizie se caută întotdeauna materiale cu performanțe cât mai constante în diferite domenii de temperatură. Materialele cu o anomalie de densitate și o rețea cubică sunt deosebit de potrivite , deoarece au expansiune termică izotropă negativă, adică Aceasta înseamnă că expansiunea lor este aceeași în toate cele trei direcții spațiale. Exemplele includ , și . În timp ce peste un interval de temperatură de la 0,3 la 1050 K are expansiune termică negativă, este evidentă și anomalia densității, însă, doar în faza lor de temperatură ridicată începând de la 350 până la 400 K.
Totuși, poate fi utilă și proiectarea materialelor cu o dilatare termică precis definită. În cazul implanturilor dentare , este important ca umplutura să nu se extindă semnificativ mai mult sau mai puțin odată cu temperatura. B. ia o băutură caldă sau rece . Prin urmare, poate fi avantajos să se potrivească extinderea generală a implantului cu expansiunea dinților prin utilizarea de materiale cu dilatare termică pozitivă și negativă .
Exemple
apă
La presiune normală , apa are cea mai mare densitate de aproximativ 1000 de kilograme pe metru cub la 3,98 ° C și este lichidă. Sub 3,98 ° C, apa se extinde (din nou) când temperatura scade (mai departe) - chiar și atunci când se transformă în stare solidă. Anomalia apei există astfel în intervalul cuprins între 0 ° C și 3,98 ° C, gheața nu se comportă anormal, chiar dacă densitatea gheții este netipic mai mică decât cea a apei lichide. Cele mai precise valori publicate în prezent pentru densitatea maximă sunt (999,974950 ± 0,00084) kg / m 3 la o temperatură de (3,983 ± 0,00067) ° C. Valorile reprezintă o medie a cifrelor publicate de diferite institute fizice (începând cu 2005).
Calculul densității apei fără aer D LF în funcție de temperatura T ([ T ] = ° C) se poate face cu ajutorul următoarei ecuații viriale :
- .
cu coeficienții: a 0 = 999.83952; a 1 = 16,952577 (° C) -1 ; a 2 = −7.9905127 · 10 −3 (° C) −2 ; a 3 = −4.6241757 · 10 −5 (° C) −3 ; a 4 = 1,0584601 · 10 −7 (° C) −4 ; a 5 = −2.8103006 · 10 −10 (° C) −5 și b = 0,016887236. Pentru calcularea densității apei saturate cu aer este corectat la valoarea D LG / (g / l) = D LF / (g / l) - 0.004612 + 0,000106 (° C) -1 · T .
În starea solidă de agregare - în acest caz gheață - se obține în mod normal o ordine pe distanțe mari prin formarea unei rețele de cristal în cursul cristalizării . În stare lichidă există un amestec de ordine și haos, moleculele umplând un volum mai mare datorită vitezei lor mai mari . Deci volumul crește și densitatea scade. În starea gazoasă se atinge tulburarea maximă, adică H. în consecință, moleculele sunt distribuite uniform pe spațiul maxim disponibil.
Motivul anomaliei apei constă în înlănțuirea moleculelor de apă prin legături de hidrogen . Ca urmare, structura necesită mai mult spațiu în stare solidă decât în cazul moleculelor mobile. Formarea structurii este un proces progresiv, ceea ce înseamnă că așa-numitele grupuri de molecule de apă sunt deja prezente în stare lichidă . La 3,98 ° C, se ajunge la starea în care grupurile individuale ocupă cel mai mic volum și, astfel, au cea mai mare densitate. Dacă temperatura scade și mai mult , este necesar un volum mai mare datorită schimbării constante a structurilor cristaline . Când temperatura crește, moleculele au nevoie din nou de mai multă libertate de mișcare, ceea ce crește și volumul.
Durata de viață a grupurilor individuale depinde de temperatură și este de doar câteva trilioane de secundă la 4 ° C. Odată cu răcirea ulterioară, starea instabilă a clusterelor devine din ce în ce mai stabilă datorită mișcării de căldură în scădere, până când structurile cristaline hexagonale stabile s-au format în final (gheață) în timpul solidificării. Volumul crește din nou semnificativ în timpul acestei tranziții de fază.
Anomalia densității apei este importantă pentru viața în apele climatelor mai reci. Apa de suprafață nu scufundă sub o temperatură de aproximativ 4 ° C. În loc de răcirea asociată a straturilor de apă mai adânci și înghețarea completă de dedesubt, se pot forma straturi termice . Animalele și plantele acvatice pot supraviețui sub stratul de gheață.
Temperatura la care apa atinge cea mai mare densitate scade odată cu creșterea presiunii de la 3,98 ° C (1 bar) peste aproximativ 2 ° C (100 bar) până la aproximativ 0 ° C (200 bari, în care punctul de îngheț în sine este aici) are a scăzut la -1,5 ° C).
Valori numerice pentru anomalia densității și coeficientul de expansiune al gheții și apei la presiune normală
Coeficientul de expansiune calculat este un coeficient mediu de expansiune între cele două temperaturi.
| substanţă | / în [° C] | / în [g / cm³] | în [K] | temperatura medie în [° C] | în [1 / K] | surse |
|---|---|---|---|---|---|---|
| apă | 0/0 | 0,918 (gheață) / 0,999840 (apă) | 0 | 0 | - | , |
| 0/1 | 0,918 (gheață) / 0,999899 | 1 | 0,5 | -0.0819 ! | ||
| 0/1 | 0,999840 (apă) / 0,999899 | 1 | 0,5 | −0,000059006 | ||
| 1/2 | 0,999899 / 0,999940 | 1 | 1.5 | -0,0000410025 | ||
| 2/3 | 0,999940 / 0,999964 | 1 | 2.5 | -0.0000240009 | ||
| 3 / 3.983 (densitate maximă!) | 0,999964 / 0,999975 | 0,983 | 3.4915 | -0.0000119051 | ||
| 3/4 | 0,999964 / 0,999972 | 1 | 3.5 | -0.00000800023 | ||
| 3.983 (densitate maximă!) / 4 | 0,999975 / 0,999972 | 0,017 | 3,9915 | +0.000176476 | ||
| 3/5 | 0,999964 / 0,999964 | 2 | 4 (aproape de densitatea maximă!) | 0 | ||
| 4/5 | 0,999972 / 0,999964 | 1 | 4.5 | +0,00000800028 | ||
| 5/6 | 0,999964 / 0,999940 | 1 | 5.5 | +0,0000240014 | ||
| 6/7 | 0,999940 / 0,999901 | 1 | 6.5 | +0.0000390039 | ||
| 17/19 | 0,998773 / 0,998403 | 2 | 18 | +0.0001853 | ||
| 19/21 | 0,998403 / 0,997991 | 2 | 20 | +0.0002064 | ||
| 24/26 | 0,997295 / 0,996782 | 2 | 25 | +0.0002573 |
Dacă gheața se topește în apă la 0 ° C, volumul acesteia scade cu aproximativ 8,19%. La îngheț, crește corespunzător cu aproximativ 8,92%.
Coeficienții medii de expansiune au fost calculați din valorile densității:
Anomalie de densitate și coeficient de expansiune (neizobaric) al amoniacului lichid
Gazul lichid are o presiune de vapori diferită la fiecare temperatură , în funcție de funcția sa de presiune a vaporilor . Prin urmare, expansiunea sau contracția volumului legată de temperatură nu are loc izobaric.
Coeficienții de expansiune negativi sunt marcați cu caractere aldine.
Coeficientul de expansiune calculat este un coeficient mediu de expansiune între cele două temperaturi.
| substanţă | / în [° C] | / în [g / cm³] | în [K] |
temperatura medie în [° C] |
în [1 / K] | surse |
|---|---|---|---|---|---|---|
| amoniac lichid , care fierbe (la propria presiune de vapori) | −70 / −68 | 0,72527 / 0,72036 | 2 | −69 | +0,003408 | |
| −68 / −66 | 0,72036 / 0,72067 | 2 | −67 | -0.000215 | ||
| −66 / −64 | 0,72067 / 0,71839 | 2 | −65 | +0,001587 | ||
| -64 / -62 | 0,71839 / 0,71608 | 2 | −63 | +0,001613 | ||
| −50 / −48 | 0,70200 / 0,69964 | 2 | −49 | +0,001687 | ||
| −30 / −28 | 0,66764 / 0,67517 | 2 | −29 | +0,001829 | ||
| −28 / −26 | 0,67517 / 0,67263 | 2 | −27 | +0,001888 | ||
| −26 / −24 | 0,67263 / 0,67463 | 2 | −25 | -0,001482 | ||
| −24 / −22 | 0,67463 / 0,66887 | 2 | −23 | -0,008194 | ||
| −22 / −20 | 0,68587 / 0,66503 | 2 | −21 | +0.015668 | ||
| −2 / 0 | 0,64127 / 0,63857 | 2 | −1 | +0,002114 | ||
| −2 / 2 | 0,64127 / 0,63585 | Al 4-lea | 0 | +0,002131 | ||
| 0/2 | 0,63857 / 0,63585 | 2 | 1 | +0,002139 | ||
| 18/20 | 0,61320 / 0,61028 | 2 | 19 | +0,002392 | ||
| 18/22 | 0,61320 / 0,60731 | Al 4-lea | 20 | +0,002425 | ||
| 20/22 | 0,61028 / 0,60731 | 2 | 21 | +0,002445 | ||
| 24/26 | 0,60438 / 0,60132 | 2 | 25 | +0,002544 | ||
| 48/50 | 0,56628 / 0,56306 | 2 | 49 | +0,002859 |
Notă: Valorile densității și coeficienții de expansiune ai amoniacului lichid prezintă două anomalii de densitate în intervalul de temperatură luat în considerare!
Coeficienții medii de expansiune au fost calculați din valorile densității:
Coeficienții de densitate sunt indirect proporționali cu coeficienții de volum sau cu coeficienții volumelor specifice v (volum de masă specific sau volum molar )!
Anomalie de densitate și coeficient de expansiune a litiului topit
Vezi: Coeficient de expansiune # Valori numerice ale metalelor topite .
Dovezi individuale
- ↑ W. Fratzscher, HP Picht: Date materiale și caracteristici ale ingineriei de proces. Verlag für Grundstoffindindustrie Leipzig, GDR 1979 / BRD 1993, date din topituri metalice, Lithium p. 176.
- ↑ http://iffwww.iff.kfa-juelich.de/~jones/PhysRevB.81.094202.pdf Variații de densitate în telurul lichid: Rolurile inelelor, lanțurilor și cavităților, p. 1.
- ↑ a b Martin T Dove, Hong Fang: expansiune termică negativă și proprietăți fizice anormale asociate: revizuirea fundamentului teoretic al dinamicii rețelelor . În: Rapoarte privind progresul în fizică . bandă 79 , nr. 6 , 1 iunie 2016, ISSN 0034-4885 , p. 066503 , doi : 10.1088 / 0034-4885 / 79/6/066503 ( iop.org [accesat la 11 martie 2020]).
- ↑ Koshi Takenaka: Materiale negative de expansiune termică: cheie tehnologică pentru controlul expansiunii termice . În: Știința și tehnologia materialelor avansate . bandă 13 , nr. 1 , februarie 2012, ISSN 1468-6996 , p. 013001 , doi : 10.1088 / 1468-6996 / 13/1/013001 ( tandfonline.com [accesat la 11 martie 2020]).
- ↑ R. Mittal, SL Chaplot: Calcul dinamic al rețelei de expansiune termică negativă în ZrV 2 O 7 și HfV 2 O 7 . În: Physical Review B . bandă 78 , nr. 17 , 7 noiembrie 2008, ISSN 1098-0121 , p. 174303 , doi : 10.1103 / PhysRevB.78.174303 ( aps.org [accesat la 11 martie 2020]).
- ↑ Tetsuo Hisashige, Teppei Yamaguchi, Toshihide Tsuji, Yasuhisa Yamamura: tranziția de fază a soluțiilor solide Zr1-xHfxV2O7 având expansiune termică negativă . În: Jurnalul Societății de Ceramică din Japonia . bandă 114 , nr. 1331 , 2006, ISSN 0914-5400 , p. 607–611 , doi : 10.2109 / jcersj.114.607 ( jst.go.jp [accesat la 11 martie 2020]).
- ↑ Comunicații PTB 100 / 3-90: Horst Bettin și Frank Spieweck: Densitatea apei în funcție de temperatură după introducerea scării internaționale de temperatură în 1990. PTB-Mitteilungen 100 3/90, (1990) pp. 195- 196.
- ↑ tec-science: Anomalie de densitate a apei. În: tec-science. 16 februarie 2019, accesat la 8 noiembrie 2020 (germană).
- ↑ Engineering ToolBox: Densitatea și volumul specific al unui lichid versus variația presiunii și temperaturii (engleză), 2009, accesat la 28 decembrie 2018.
- ↑ U. Hübschmann, E. Stânga: Tabelele despre chimie. Verlag Handwerk und Technik, Hamburg 1991, ISBN 3-582-01234-4 , densitatea mercurului și a apei la diferite temperaturi și presiunea aerului, p. 36.
- ↑ Formule și tabele pentru nivelurile secundare I și II. Paetec GmbH, 1996, ISBN 3-89517-253-7 , p. 11
- ↑ W. Fratzscher, HP Picht: Date materiale și caracteristici ale ingineriei de proces. Verlag für Grundstoffindindustrie Leipzig, GDR 1979 / BRD 1993, pp. 144–146 - Date termodinamice ale amoniacului, valori ale densității calculate din volume specifice v '.