cupru
| proprietăți | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| În general | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numele , simbolul , numărul atomic | Cupru, Cu, 29 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria elementului | Metale de tranziție | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup , punct , bloc | 11 , 4 , d | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Uite | roșu-maroniu, metalic, de culoare cupru | |||||||||||||||||||||||||||||||||||||||||||||||||||
| numar CAS | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numărul CE | 231-159-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA InfoCard | 100.028.326 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Fracțiune de masă din anvelopa pământului | 0,01% | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masă atomică | 63.546 (3) u | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Raza atomică (calculată) | 135 (145) pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Raza covalentă | 132 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Raza Van der Waals | Ora 140 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuratie electronica | [ Ar ] 3 d 10 4 s 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Energia de ionizare | Al 7-lea.726 380 (4) eV ≈ 745.48 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Energia de ionizare | 20.29239 (6) eV ≈ 1 957.92 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Energia de ionizare | 36.841 (12) eV ≈ 3 554.6 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Energia de ionizare | 57.38 (5) eV ≈ 5 536 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Energia de ionizare | 79.8 (7) eV ≈ 7 700 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizic | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Starea fizică | cu fermitate | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Structură cristalină | Centrat pe zonă cubică | |||||||||||||||||||||||||||||||||||||||||||||||||||
| densitate | 8,92 g / cm³ (20 ° C ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duritatea lui Mohs | 3.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| magnetism | diamagnetic ( Χ m = −9,6 10 −6 ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de topire | 1357,77 K (1084,62 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de fierbere | 2868 K (2595 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumul molar | 7,11 · 10 −6 m 3 · mol −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Căldura evaporării | 305 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Căldura de fuziune | 13,3 kJ mol −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Viteza sunetului | 3570 m s −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacitate termică specifică | 385 J kg −1 K −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Funcția de lucru | 4,65 eV | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitatea electrică | 58,1 · 10 6 A · V −1 · m −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitate termică | 400 W m −1 K −1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Mecanic | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modul de elasticitate | 100 ... 130 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Numărul lui Poisson | 0,34 ... 0,35 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Chimic | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stări de oxidare | 1, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Potențial normal | 0,340 V (Cu 2+ + 2 e - → Cu) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitate | 1.9 ( scara Pauling ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopi | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pentru alți izotopi, a se vedea lista izotopilor | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți RMN | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| instructiuni de siguranta | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAK |
Elveția: 0,1 mg m −3 (măsurat ca praf inhalabil ) |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
În măsura în care este posibil și obișnuit, sunt utilizate unități SI . Dacă nu se specifică altfel, datele furnizate se aplică condițiilor standard . | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Cuprul ( latin Cuprum ) este un element chimic cu simbolul elementului Cu și numărul atomic 29. Este un metal de tranziție , în tabelul periodic se află în a 4-a perioadă și în primul subgrup (după noul grup de numărare 11) sau cupru grup . Denumirea latină cuprum este derivată din (aes) cyprium „ minereu din insula greacă Cipru ”, unde cuprul a fost extras în antichitate.
Ca un metal relativ moale, cuprul este ușor de modelat și dur. Este folosit în multe feluri ca un excelent conductor de căldură și electricitate . În plus, aparține și grupului metalelor monede .
Ca o tehnologie importantă sau metal funcțional, cuprul este un metal semi-prețios .
istorie

Cuprul, aurul , argintul și staniul au fost primele metale pe care omenirea le-a cunoscut în dezvoltarea lor. Deoarece cuprul este ușor de lucrat, a fost folosit de cele mai vechi culturi cunoscute acum aproximativ 10.000 de ani. Momentul utilizării sale pe scară largă din mileniul V î.Hr. Până în mileniul III î.Hr. BC se mai numește Epoca cuprului , în funcție de regiune . În Hujayrat al-Ghuzlan, în Iordania, exista deja în jur de 4.000 î.Hr. Un sit de producție în masă de cupru. În alchimie , cuprul a fost asociat cu Venus și feminitatea ♀ ( metale planetare ) și privit ca un compus de sulf și mercur. Primele oglinzi au fost realizate din acest metal. În epoca târzie a bronzului mediteranean estic , cuprul a fost extras în principal în Cipru și a fost exportat de acolo în majoritatea barelor de cupru de aproximativ 30 kg sub formă de piei de bovine (așa-numitele bare de piele de bou ). Fragmente de bare de piele de cipru din secolele XVI-XI î.Hr. BC poate fi găsit în părți mari ale zonei mediteraneene, până în Sardinia, în Balcani și chiar la nord de Alpi ( depozit găsit în Oberwilflingen ). Cel mai mare producător de cupru preindustrial a fost Imperiul Roman, cu o producție anuală estimată la 15.000 de tone.
Ulterior, cuprul a fost aliat cu staniu și plumb pentru a forma bronz . Acest aliaj mai dur și mai rezistent din punct de vedere tehnic și-a dat numele epocii bronzului . Distincția dintre plumb și staniu a fost introdusă numai cu o cunoaștere tot mai mare a metalelor, astfel încât, din perspectiva actuală, termenul de bronz este aplicat corect numai aliajelor de staniu-cupru cu un conținut ridicat de cupru.
„ Alama ” din aliajul galben auriu cupru-zinc era deja cunoscut în Grecia antică . A fost topit prin prelucrarea minereurilor respective împreună, dar abia la romani acest proces a fost din ce în ce mai utilizat. Aliajul auriu-cupru Tumbaga a fost utilizat pe scară largă în Columbia antică .
Cuprul ca mineral
Aparițiile naturale ale cuprului nativ, adică în forma sa elementară, erau cunoscute cu mult înainte de înființarea Asociației Internaționale Mineralogice (IMA). Prin urmare, cuprul este recunoscut ca un așa-numit mineral bunic ca un tip independent de mineral.
Conform sistematicii mineralelor conform Strunz (ediția a IX-a) , cuprul este clasificat la sistemul nr. „1.AA.05” (elemente - metale și compuși intermetalici - familia cupalitului de cupru - grupul cuprului) sau în ediția a VIII-a învechită clasificată la I / A.01 ( seria cuprului ). Sistematica mineralelor conform Dana , care este utilizată în principal în țările vorbitoare de limbă engleză , enumeră elementul mineral sub sistemul nr. 01/01/01/03 ( grupa de aur ).
În natură, cuprul se formează de obicei în lavele bazaltice fie sub formă de „roșu-cupru”, pepite metalice lucioase (solidificate din topitură), fie în structuri ramificate, așa-numitele dendrite . Ocazional, se poate găsi și antrenament cristalin. Cuprul are loc în parageneză cu diverse, mai ales secundare minerale de cupru , cum ar fi bornit , chalcosine , cornwallite , cuprita , azurit și malachit precum tenorita , dar poate fi , de asemenea , asociat cu multe alte minerale , cum ar fi calcit , clinoclase , Prehnite , lotrit , cuarț și argintiu .
Pseudomorfism de la cupru la aragonit
Minereurile de cupru sunt comune. De exemplu, cuprul este fabricat din calcopirită ( pirite de cupru , CuFeS 2 ), calcozină ( luciu de cupru , Cu 2 S), mai rar și din bornită ( pietricele de cupru colorate , Cu 5 FeS 4 ), atacamit (CuCl 2 Cu (OH) 2 ), malachit (Cu 2 [(OH) 2 | CO 3 ]) și alte minereuri. În 2019, erau cunoscute 636 de minerale de cupru . Mineralele cu cea mai mare concentrație de cupru din compus sunt cupritul (până la 88,8%) și algodonitul (până la 83,6%), precum și paramelaconitul , tenoritul și calcozina (până la 79,9%).
Apariție și extracție
Potrivit Institutului German al Cuprului, cuprul apare pe pământ cu un conținut de aproximativ 0,006% și se află pe locul 23 în ceea ce privește frecvența elementelor din scoarța terestră . Adesea cuprul apare sub formă solidă , adică sub formă elementară. La nivel mondial (începând cu 2017) există în prezent (începând cu 2017) peste 3000 de locații cunoscute pentru cuprul solid, inclusiv în Afganistan , Argentina , Australia , Belgia , Bolivia , Brazilia , Bulgaria , Chile , China , Republica Democrată Congo , Germania , Finlanda , Franța , Grecia , India , Iran , Irlanda , Italia , Japonia , Canada , Kazahstan , Maroc , Mexic , Mongolia , Namibia , Noua Zeelandă , Norvegia , Austria , Peru , Filipine , Polonia , Portugalia , România , Rusia , Zambia , Suedia , Elveția , Zimbabwe , Slovacia , Spania , Africa de Sud , Republica Cehă , Turcia , Ucraina , Ungaria , Statele Unite ale Americii (SUA) și Regatul Unit (Regatul Unit).
Cuprul solid ar putea fi, de asemenea, detectat în mai multe eșantioane de roci de pe creasta Atlanticului mijlociu și din lună , pe care sonda misiunii Luna 24 a adus-o de la Mare Crisium .
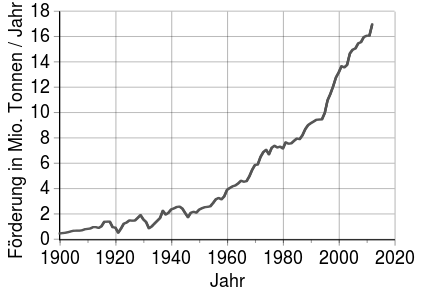
Promovare și rezerve
Cel mai important producător de cupru este Chile, urmat de un drum lung de Peru și China. În Europa, Polonia , Portugalia și Suedia sunt de remarcat. Cele mai importante țări exportatoare au fost organizate în CIPEC între 1967 și 1988 . CIPEC a inclus Chile, Peru și Papua Noua Guinee , pe a cărei insulă Bougainville una dintre cele mai mari mine de cupru din lume a dus la un război civil în 1988.
Minele de cupru din Peninsula Keweenaw din Lacul Superior (SUA) au fost semnificative din punct de vedere istoric . Acolo era cel mai mare zăcământ de cupru din lume. Exploatarea minieră avea loc acolo în epoca precolumbiană. În Germania, șistul de cupru a fost exploatat în regiunea Mansfeld până în 1990 . Alte situri miniere istorice au fost Kupferberg / Franconia Superioară (din secolul al XIII-lea) și Silezia de Jos Kupferberg / Riesengebirge (din secolul al XII-lea) .În Cornwall (Anglia) a existat o exploatare semnificativă a cuprului, în special în secolele al XVIII-lea și al XIX-lea.
Potrivit Grupului Internațional de Studiu asupra Cuprului ICSG, conform Studiului Geologic al Statelor Unite (USGS), rezervele de cupru sunt în prezent în jur de 870 milioane tone (Mt). Resursele de cupru identificate și nedescoperite sunt estimate la aproximativ 2.100 Mt și respectiv 3.500 Mt pentru un total de 5.600 Mt. Acesta din urmă nu ia în considerare cantitățile uriașe de cupru care se află în noduli de adâncime și sulfuri masive de pe uscat și submarine.
| rang | țară | avansare | Rezerve |
|---|---|---|---|
| 1 | Chile | 5800 | 170.000 |
| 2 | Peru | 2400 | 83.000 |
| 3 | Republica Populară Chineză | 1600 | 26.000 |
| Al 4-lea | Statele Unite | 1200 | 48.000 |
| 5 | Republica Democrată Congo | 1200 | 20.000 |
| Al 6-lea | Australia | 950 | 88.000 |
| Al 7-lea | Zambia | 870 | 19.000 |
| A 8-a | Indonezia | 780 | 51.000 |
| 9 | Mexic | 760 | 50.000 |
| 10 | Rusia | 710 | 61.000 |
Extracţie
Cupru brut
Cele mai importante cuptoare pentru extracția cuprului sunt cuptorul cu flacără și, din 1980, topitorul cu bliț .
Pentru producția de cupru, așa-numita piatră de cupru (Cu 2 S cu conținut variabil de FeS și un conținut de Cu de aproximativ 70%) este mai întâi extrasă din pirite de cupru (CuFeS 2 ) . În acest scop, materia primă este prăjită cu adăugarea de cocs, iar oxizii de fier conținuți sunt zgurați cu agregate care conțin silice . Această zgură de silicat de fier plutește pe piatra de cupru și poate fi astfel turnată cu ușurință.
- Lucrări de prăjire:
- Lucrul de topire:
Piatra de cupru obținută în acest mod este prelucrată în cupru brut (cunoscut și sub numele de cupru negru ). Pentru a face acest lucru, este turnat într-un convertor și aerul este suflat în această topitură. Într-o primă etapă (bule de zgură) , sulfura de fier conținută în acesta este prăjită în oxid de fier și aceasta este legată de cuarț zgura pentru a forma zgură, care poate fi turnată. În a doua etapă (bule de gătit) , două treimi din Cu 2 S rămas se oxidează la Cu 2 O. Oxidul reacționează apoi cu sulfura rămasă pentru a forma cupru brut.
- Bule de zgură:
- Bule de gătit:
Cuprul brut are un conținut de cupru de 98%. Pe lângă metalele de bază precum fierul și zincul, restul de 2% conține și metale prețioase precum argintul și aurul.
Rafinare
Rafinarea electrolitică a cuprului se realizează într - o soluție de cupru (II) sulfat conținând acid sulfuric cu cupru brut anod și un cupru pur catod . În timpul electrolizei, toate metalele care sunt mai puțin nobile decât cuprul sunt oxidate și intră în soluție ca cationi , în timp ce metalele mai nobile se scufundă ca nămol de anod .
Ecuația de reacție a rafinării electrolitice:
- anod
- catod
În timp ce anodul se dizolvă încet odată cu formarea cationilor, numai cuprul, cuprul electrolitic, cu o fracție de masă de w (Cu) = 99,99% se depune pe catod datorită reducerii ionilor de cupru .
Nămolul anodic care este creat ca produs secundar este reciclat ulterior și servește ca materie primă pentru extracția metalelor prețioase.
Cuprul este extras în rafinării . În Europa, Aurubis AG (fostă Norddeutsche Affinerie) cu sediul în Hamburg este cunoscută pentru acest lucru și a fost Duisburger Kupferhütte (astăzi DK Recycling und Pig font ).
Cuprul poate fi obținut și ca așa-numitul cupru de ciment prin precipitare din soluție de sulfat de cupru cu fier . Procesul de precipitații se numește cimentare . Cuprul obținut este adesea contaminat. Precipitarea cuprului pe fier din soluțiile naturale de sare metalică se practică în China încă din 1086 d.Hr.
Cuprul poate fi reprezentat și de o reacție aluminotermică . Ca termit se folosește un amestec de oxid de cupru (II) și granule de aluminiu . Prin utilizarea unui superplasticizant (de exemplu, fluorură de calciu ), randamentul poate fi crescut deoarece metalele elementare, spre deosebire de zgura rezultată, nu se pot dizolva în superplastifiant. Extracția aluminotermică nu este economică din cauza aluminiului necesar pentru aceasta.
proprietăți
O bună conductivitate electrică și termică sunt proprietăți importante ale cuprului ca material. Marea importanță a acestui material pentru tehnologie provine din combinarea diferitelor proprietăți bune care - de asemenea, în legătură cu alte metale sub formă de aliaje de cupru - au fost utilizate și dezvoltate în continuare de ani de zile. În plus, cuprul are o rezistență excelentă la coroziune și este 100% reciclabil fără pierderi de calitate.
Proprietăți fizice

Datorită densității sale de 8920 kg / m³, cuprul este unul dintre metalele grele , care cristalizează într-o manieră cubică centrată pe față și are astfel un ambalaj cubic cel mai apropiat de sfere cu grupul spațial Fm 3 m (grup spațial nr. 225) . Parametrul zăbrele pentru cupru pur este 0.3615 nm (corespunde 3,615 Å ) cu 4 unități de formula per unitate de celule .
Cuprul este un foarte bun conductor de căldură . Punctul său de topire este de 1083,4 ° C. Cuprul este, de asemenea, un conductor electric foarte bun cu o conductivitate electrică de 58 · 10 6 S / m. Conductivitatea sa este doar puțin mai slabă decât argintul și semnificativ mai bună decât aurul . Deoarece toate amestecurile dizolvate în cupru, în special impuritățile precum fosforul și fierul, reduc foarte mult conductivitatea, cele mai înalte grade de puritate sunt adesea utilizate pentru materialele conductoare ( Cu-ETP , anterior E-cupru, 99,9% puritate).
Duritate Mohs de cupru este de 2,5 până la 3, care corespunde unei duritate Vickers (VHN) de 77-99 , cu o forță de încercare de 1N. Prin formarea la rece, care are o rezistență la tracțiune de 150 până la 200 MPa (moale) crescută la> 350 MPa. Elongația la rupere este redusă la sub 5% , cu valori de duritate în jur de 100 HB . Conductivitatea scade. Cuprul deformat și apoi recoacut moale are o alungire la rupere> 40% și valori de duritate în jur de 50 HB.
Moliciunea cuprului explică parțial ridicată sale conductivitate electrică și de înaltă conductivitate termică , care este a doua cea mai mare printre pure metale , la temperatura camerei , după argint . Acest lucru se datorează faptului că rezistivitatea pentru transportul electronilor în metale la temperatura camerei , se bazează în principal pe împrăștierea de electroni în timpul termici vibrațiilor zăbrele , care sunt relativ slabe într - un soft de metal .
Forjarea este foarte posibilă la temperaturi de 700 până la 800 ° C. Formarea la rece poate fi efectuată fără recoacere intermediară , se produce întărirea prin deformare .
Ca metal gol , cuprul are o culoare roșie deschisă, culoarea liniei este roz-roșu. Culoarea roșie provine din faptul că acesta absoarbe complementară verde și albastru lumina un pic mai mult la normal de temperatură . Se pătează atunci când este expus la aer și devine inițial roșu-maro. Odată cu degradarea și coroziunea suplimentară , suprafața netedă se pierde foarte lent (adesea de-a lungul secolelor) și culoarea se schimbă de la roșu-maroniu la albastru-verde datorită formării unei patine . Cuprul este un material de construcție durabil cu o „speranță de viață” tehnică de peste 200 de ani. Această rezistență se bazează pe capacitatea sa de a forma un strat de protecție rezistent la intemperii, care aderă ferm în atmosferă. Acest strat de oxid este inerent stabil și „auto-vindecat”. Indiferent de compoziția sa, oferă protecție împotriva atacurilor corozive suplimentare.
Cuprul este unul dintre puținele elemente metalice cu o culoare naturală diferită de gri sau argintiu. Suprafețele de cupru pur sunt roșii somon și devin maro roșiatic în aer . Culoarea caracteristică a cuprului rezultă din tranzițiile între benzi ale electronilor prezenți în orbitalul atomului d .
Ca și în cazul altor metale , coroziunea galvanică apare atunci când cuprul este adus în contact cu alt metal într- un electrolit . Formează elemente locale , de exemplu ca o componentă de urmărire în zinc. Cu toate acestea, ca metal relativ nobil din seria electrochimică , acesta nu este afectat de coroziune.
Proprietăți chimice
| Stări de oxidare ale cuprului | |
|---|---|
| +1 | CuCI , Cu 2 O , CuH , Cu 2 C 2 |
| +2 | CuCI 2 , CuO , CuSO 4 , cupru (II) acetat de |
| +3 | KCuO 2 , K 3 CuF 6 |
| +4 | Cs 2 CuF 6 |
Cuprul apare în stările de oxidare 0, +1, +2, +3 și +4, cele mai frecvente fiind +1 și +2, +2 fiind cea mai stabilă stare de oxidare în soluțiile apoase ; Nivelul +4 este extrem de rar (de exemplu în Cs 2 CuF 6 ). Sărurile de cupru (II) (de exemplu, sulfatul de cupru ) sunt de obicei de culoare albastră sau verde. În termeni chimici , cuprul are în unele cazuri proprietăți similare cu elementele argint și aur, care se află în același grup . Un strat de cupru metalic este depus pe un cui de fier care este scufundat într-o soluție de sulfat de cupru , pentru care fierul intră în soluție ca sulfat de fier , deoarece fierul este mai puțin nobil decât cuprul (vezi și seria de tensiune ). Cuprul nu este în mod normal atacat de acid clorhidric , ci este puternic atacat în prezența oxigenului ; este dizolvat de acid sulfuric fierbinte . De asemenea, se dizolvă în acid azotic și aqua regia . Un amestec de acid clorhidric sau acid sulfuric cu peroxid de hidrogen dizolvă cuprul foarte repede. Metalul este de asemenea atacat de acizi organici . Împotriva alcalinilor este stabil. În căldură roșie reacționează cu oxigenul și formează un strat gros de oxid de cupru . Cuprul este pasivat de fluor și de compușii săi . În funcție de mărimea bobului , pulberea de cupru este inflamabilă sau combustibilă . Metalul în formă compactă nu este combustibil și, după formarea unui subțire strat de oxid de aer și apă nu a atacat, așa că este împotriva aer curat și apă rezistent .
In lichid cupru se dizolvă oxigen și hidrogen , care în solidificare a topiturii la vaporii de apă să fie în măsură să pună în aplicare și , astfel , cauza porozitatii gazului în turnare sub forma.
Fisurile și cavitățile pot apărea în clasele de cupru care conțin oxigen atunci când vin în contact cu gazele care conțin hidrogen , ceea ce duce la ceea ce este cunoscut sub denumirea de fragilitate de hidrogen în cupru .
Proprietăți biologice
Pentru organismul uman, cuprul este un oligoelement esențial , adică oamenii au nevoie de cupru pentru a supraviețui. Necesarul zilnic de aproximativ 2 mg pentru un adult este de obicei atins prin consumul unei diete echilibrate cu o proporție mare de cereale, carne, legume rădăcinoase, leguminoase, nuci sau chiar ciocolată. Cuprul este un element natural care poate fi găsit sub diferite forme și concentrații în scoarța terestră, oceane, lacuri și râuri. Viața florei și a faunei a evoluat în cadrul acestei prezențe naturale a cuprului. Prin urmare, majoritatea organismelor au un mecanism intrinsec pentru utilizarea lor.
Proprietăți antimicrobiene
Cuprul este toxic pentru multe microorganisme (viruși, germeni) chiar și în concentrații scăzute. Datorită proprietății antimicrobiene a cuprului, materialul este z. B. utilizat în experimente la scară largă în spitale. Un studiu clinic din 2008/2009 arată că în Clinica Asklepios din Wandsbek , Hamburg, după înlocuirea a 50 de mânere / plăci și întrerupătoare de lumină, germenii MRSA au fost reduși la 63%. Un studiu din Chile a constatat o reducere a numărului de germeni pe obiectele din aliaje de cupru cu până la 92% la o umiditate cuprinsă între 7,2 și 19,7%. Un studiu multicentric din 2010/2011 din SUA arată că rata infecției în „încăperile din cupru” scade cu aproape 60%, iar numărul de germeni pe obiectele din cupru a fost redus cu peste 80%. În 2013, Clinica de Medicină Pediatrică și a Adolescenților din Clinica Niederberg din Renania de Nord-Westfalia și-a schimbat mânerele ușii cu cele din aliaj de cupru. Sunt necesare aliaje cu mai mult de 60% cupru. În SUA sunt în curs alte studii cu diferite aplicații de cupru.
Experimentele sugerează că uciderea prin contact are loc printr-un mecanism în care contactul metalic-bacterian dăunează învelișului celulei, ceea ce, la rândul său, face celulele susceptibile la deteriorarea ulterioară a cuprului. În prezent, există trei experimente ale grupului de lucru pe stația spațială ISS și vor urma încă câteva.
Efectul de reducere a germenilor rezultă din faptul că ionii de cupru se leaga la tiol grupe de proteine și peroxida lipidelor ale membranei celulare , care duce la formarea de radicali liberi care deteriorează din ADN - ul membranelor și celulare. La om, de exemplu, în cazul bolii Wilson (boala de stocare a cuprului), aceasta duce la deteriorarea organelor cu un exces mare de cupru.
Aliajele de cupru cu un conținut de cupru de cel puțin 60% prezintă, de asemenea, un efect toxic împotriva norovirusurilor .
Efect împotriva melcilor
Cuprul din firul de cupru sau folia de cupru, care servește drept barieră pentru plantele pe cale de dispariție, este oxidat de nămolul melc. Aceasta creează o substanță iritantă care împiedică melcul să se târască mai departe.
Cererea biologică de cupru
Deoarece cuprul este deosebit de important pentru metabolism, o deficiență de cupru poate duce la probleme grave de sănătate. Beneficiile cuprului pentru sănătate sunt numeroase, deoarece cuprul influențează multe funcții ale corpului ca o componentă a enzimelor și proteinelor vitale: Cuprul este esențial pentru creșterea sugarilor, rezistența osoasă, maturarea celulelor roșii și albe din sânge, transportul fierului, colesterolului și glucozei metabolismul, contracția mușchilor inimii și dezvoltarea creierului.
Necesarul zilnic al unui adult este de 1,0-1,5 miligrame. În corpul uman, cuprul este stocat în principal în ficat.
Cuprul se găsește în principal în ciocolată, ficat, cereale, legume și nuci. Deficitul de cupru apare rar la om. O deficiență este posibilă în special în cazul diareei de lungă durată, a copiilor precoce, după malnutriție sau malabsorbție de lungă durată din cauza unor boli precum B. sprue , boala Crohn sau fibroza chistică . Ingerarea unor doze mari de zinc , fier sau molibdat poate duce, de asemenea, la scăderea nivelului de cupru din organism. Boala Menkes este o afectiune congenitala rara a metabolismului cuprului.
Exces de cupru și otrăvire
Excesul de cupru este eliberat în sistemul digestiv cu bila pentru excreție.
Sulfatul de cupru (vitriolul de cupru) este un emetic puternic și, prin urmare, a fost utilizat pentru a trata multe otrăviri , de exemplu din fosforul alb , care, în acest caz special, are și avantajul că fosforul este legat în același timp ca fosfură de cupru slab solubilă .
În boala ereditară rară a bolii Wilson , excreția de cupru este afectată și există o acumulare crescută de cupru, mai întâi în ficat, apoi, atunci când acesta excretă cuprul în sânge, de asemenea, în alte organe. O altă boală la fel de rară a metabolismului cuprului este sindromul Menkes . Cuprul poate fi absorbit de celule, dar nu mai poate fi transportat în mod ordonat, astfel încât unele organe au un conținut crescut de cupru, în timp ce altele au un conținut redus de cupru.
Cuprul și boala Alzheimer
Legătura dintre cupru și dezvoltarea bolii Alzheimer a fost discutată din nou și din nou . Încă din 2003, cercetătorii au suspectat că cuprul încetinește producția de amiloid A și că un deficit de cupru promovează boala Alzheimer. Cu toate acestea, un studiu pilot ulterior cu 70 de pacienți cu Alzheimer nu a putut arăta niciun efect protector de la un aport crescut de cupru, chiar dacă a existat o stabilizare a scăderii Abeta42 în LCR , un marker al bolii Alzheimer.
Alte studii au arătat că cuprul ar putea fi dăunător creierului . Un studiu cu ionoforul PBT2 ca ingredient activ împotriva bolii Alzheimer a arătat rezultate bune într-un studiu de fază II. Ingredientul activ leagă nu numai zincul , ci și cuprul și astfel reduce concentrația de cupru din creier.
Un nou studiu arată că cuprul se depune în capilarele creierului cu un aport ridicat pe termen lung și poate deteriora bariera hematoencefalică de acolo . Acest lucru împiedică îndepărtarea beta-amiloidului , acumularea substanței cauzând apoi boala Alzheimer .
utilizare


Cuprul este utilizat pur sau ca aliaj, în special datorită conductivității sale electrice și termice excelente , dar și datorită procesabilității și longevității sale excelente, într-un număr mare de aplicații și în multe industrii diferite, cum ar fi ingineria auto sau mecanică. Energiile regenerabile sunt acum și un domeniu important de aplicare (cuvânt cheie: clădire verde). Aceasta include, de asemenea, domenii precum telecomunicații, arhitectură, energii convenționale, instalații sanitare, încălzire, trafic, aplicații maritime, electrotehnică (de exemplu, instalații electrice ), piese de precizie, monede , tacâmuri , obiecte de artă, instrumente muzicale și multe altele.
Dacă este utilizat în contact cu alte metale, acesta duce la coroziunea de contact atunci când este expus la umiditate .
După argint, cuprul are a doua cea mai mare conductivitate electrică dintre toate substanțele, înaintea aurului și, prin urmare, este un. folosit pentru:
- linii electrice , fire jumper și cabluri de alimentare cu secțiuni transversale mici, linii aeriene
- Piste conductoare pe plăci de circuite imprimate și parțial în circuite integrate
- Mașini electrice: înfășurări de sârmă în transformatoare , bobine / bobine și motoare electrice
- Componente: corpuri anodice ale magnetronilor , cleme , picioare de conectare a componentelor, suporturi de contact, manșoane de compresie
Este adevărat că aluminiul este mai ieftin și, în termeni de masă pe lungime, un conductor electric mai bun decât cuprul. Dar este mai voluminoasă. In absenta. Din această cauză și, de asemenea, pentru că cuprul poate fi contactat mai bine și are o rezistență la oboseală la flexiune mai mare, este de obicei preferat ca conductor al aluminiului, cu excepția cazului în care greutatea sau prețul sunt importante.
Sârmele și firele din așa-numitul cupru fără oxigen ( OFC , engleză pentru cupru fără oxigen cu o puritate de> 99,99%) au o structură cristalină cu granulație foarte fină și o rezistență deosebit de mare la oboseală. Sunt utilizate pentru cabluri și fire care sunt supuse unor solicitări mecanice ridicate.
Aliajele de cupru și magneziu sunt utilizate pentru liniile aeriene . Trebuie găsit un compromis între creșterea rezistenței la tracțiune și scăderea conductivității.
Cuprul are o reflectivitate ridicată în domeniul infraroșu și, prin urmare, este utilizat ca oglindă pentru razele laser cu dioxid de carbon și pentru acoperirea sticlei ( sticlă izolatoare ).
Datorită conductivității sale termice ridicate și rezistenței la coroziune, este foarte potrivit ca material pentru schimbătoare de căldură , chiuvete de căldură și plăci de montare pentru semiconductori de putere . Este adesea folosit ca vase în gastronomie .
În artă și meserii , tablele de cupru sunt antrenate , adică deformate prin ciocănire, ceea ce este ușor posibil datorită moliciunii sale. În artele plastice, cuprul este încă utilizat pentru fabricarea plăcilor de imprimare pentru gravuri și gravuri pe plăci de cupru .
Acoperișurile sunt de asemenea acoperite cu folie de cupru, care apoi formează un verzui permanent patină , care constă din diverse bază hidroxizi de cupru sau carbonați de cupru . Această patină, care este adesea denumită în mod incorect ca "verdigris" (vezi acetat de cupru ), protejează metalul de dedesubt împotriva coroziunii ulterioare , astfel încât acoperișurile din cupru pot avea o durată de viață de câteva secole. Cuieurile din cupru sunt utilizate în acoperișurile tradiționale din ardezie . Cuprul este din ce în ce mai utilizat pentru acoperișuri și fațade, tot din motive estetice.
Aliaje
Cuprul este, de asemenea, o componentă a mai mult de 400 de aliaje, cum ar fi B. alamă (cu zinc), bronz (cu tablă) și nichel argintiu (cu zinc și nichel). Aceste aliaje de cupru sunt utilizate pe scară largă datorită proprietăților lor bune, cum ar fi culoarea, rezistența la coroziune și procesabilitatea. Se face distincția între aliajele forjate (alamă și nichel argintiu) și materialele turnate ( gunmetal , bronzuri): aliajele forjate sunt aduse în forma dorită prin formarea plasticului (formare la cald: laminare, forjare etc. sau formare la rece: tragere de sârmă, ciocănire, laminare la rece, tragere adâncă etc.), în timp ce materialele turnate sunt de obicei dificile sau imposibil de format din plastic.
În funcție de adăugarea de nichel , culoarea cuprului dispare și se formează aliaje rezistente la coroziune de culoare gălbuie până la alb ( cupru-nichel ).
Multe materiale pentru monede sunt realizate pe bază de cupru, astfel încât metalul părților aurii ale monedelor euro numite „ aur nordic ” este un aliaj cupru-zinc-aluminiu-staniu. Monedele metalice ale monedelor de 1 DM valabile până în 2001 și părțile de culoare deschisă ale monedelor euro constau din aliaje cupronickel .
Compușii de cupru sunt utilizați în pigmenții de culoare , ca tonere , în preparatele medicale și în acoperirile de suprafață galvanice .
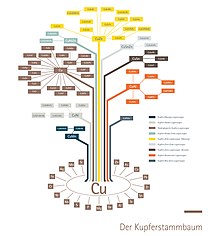
Arborele genealogic din cupru al Institutului German al Cuprului oferă o prezentare generală a diferitelor familii de aliaje.
dovada

Cuprul colorează perla borax în zona de flacără oxidantă de la albastru la verde-albastru, în zona de flacără reducătoare nu se observă decolorare sau perla este de culoare roșie până la roșu-maro. În procesul clasic de separare a cationilor , cuprul este precipitat în grupul hidrogen sulfurat și detectat acolo ca un complex albastru în grupul cuprului. Cea din urmă culoare se bazează pe faptul că soluțiile ionilor de cupru (II) cu amoniac formează un complex de tetrammină de cupru albastru intens, [Cu (NH 3 ) 4 ] 2+ (vezi și reacția de formare a complexului ).
O soluție de hexacianoferat de potasiu (II) precipită ioni de cupru (II) sub formă de hexacianoferat de cupru (II) (II), Cu 2 [Fe (CN) 6 ]. Această reacție de detectare este foarte sensibilă; adică indică și niveluri scăzute de cupru.
Sărurile de cupru colorează flacăra (flacăra arzătorului Bunsen) de la verde la albastru ( culoarea flăcării , analiză spectrală ).
Determinarea cantitativă poate fi efectuată prin electrogravimetrie pe un catod cu plasă de platină dintr-o soluție care conține acid sulfuric, cupru (II). Cuprul poate fi determinat dimensional prin iodometrie sau complexometrie ( titrare cu Titriplex / complexon III cu indicator de murexid ). În zona de cale care este disponibilă Differenzpulspolarographie (potențial pe jumătate de undă -0,62 V vs. SCE în soluție de tiocianat 1 M ). Urmele ultra de cupru sunt determinate prin voltametrie inversă , tub de grafit AAS sau ICP-MS .
Ionii de cupru (II) formează un complex albastru cu cuprizonă (acid oxalic bisciclohexiliden hidrazidă ) într-o soluție slab alcalină.
link-uri
Oxizi și hidroxizi
Oxidul de cupru (I) este roșiatic și are o structură cristalină cubică cu grupul spațial Pn 3 m (grupul spațial nr. 224) . Se folosește ca pigment în sticlă , ceramică , smalț , glazură de porțelan și ca ojă de sticlă optică , insecticid , catalizator pentru producerea de amoniac , solvent pentru minereuri de fier cromat , în electrozi galvanici , în pirotehnie , formarea norilor , inhibitori de coroziune , procese de zincare , electronice , textile , ca ignifug , aditiv combustibil, Catalizator utilizat în controlul poluării, imprimare și fotocopiere și ca conservant pentru lemn .
Oxidul de cupru (II) este un solid negru, amorf sau cristalin și formează o structură cristalină monoclinică cu grupul spațial C 2 / c (grupul spațial nr. 15) . Se utilizează în industria ceramicii pentru colorarea ochelarilor , glazurilor și emailurilor albastre, verzi sau roșii. Este folosit ocazional pentru a încorpora aditivi minerali pentru a proteja împotriva deficitului de cupru în hrana animalelor. Celelalte aplicații ale sale includ pregătirea soluțiilor pentru industria celulozei.
Cupru (II) , hidroxid este albastru și este utilizat pentru producția de pulpă , electrozi de baterii utilizate și alte săruri de cupru. Este folosit ca agent de pansament în vopsire , ca pigment și aditiv pentru hrana animalelor , în tratamentul putregaiului de depozitare în afine și ca fungicid împotriva punctelor slabe bacteriene din salată, piersici, afine și nuci.
Halogenuri
Clorura de cupru (II) este o pulbere maro, foarte higroscopică . Acesta este utilizat ca un catalizator pentru organici și anorganici reacții , mordant pentru vopsirea și imprimarea de textile , pigment pentru sticlă și ceramică , de conservare a lemnului , dezinfectant , insecticid , fungicid și erbicid , precum și catalizator în producerea de clor din acid clorhidric gazos folosit . Clorura de cupru (II) dihidrat (CuCl 2 · 2 H 2 O) este un solid albastru-verde .
Clorură de cupru (I) este de culoare albă și are o structură cristalină a blendă de zinc tip cu grupa de spațiu F 4 3 m (grup spațial nr. 216) . Este folosit ca catalizator pentru multe reacții organice . Soluțiile de amoniac de clorură de cupru (I) sunt utilizate pentru purificarea gazelor din monoxid de carbon .
Alți compuși anorganici
Sulfatul de cupru apare în mod natural sub formă de calcantit (sulfat de cupru pentahidrat, Cu [SO 4 ] · 5H 2 O) și ca boothit (sulfat de cupru heptahidrat, Cu [SO 4 ] · 7H 2 O). Este utilizat pentru conservarea pieilor pentru tăbăcire de piele , pentru producerea de săruri de cupru, pentru conservarea pasta de lemn și sol pastă de lemn , pentru a combate creșterea algelor în apă stătătoare . Este, de asemenea, utilizat în soluții de galvanizare , vopsele de spălare și marcare a metalelor, rafinării de petrol , pirotehnică și multe alte aplicații industriale .
Compusi organici

Acetat de cupru (II) (verdigris) formează cristale de culoare verde închis . Este folosit ca fungicid , catalizator pentru reacții organice , pigment pentru ceramică , insecticid , inhibitor al mucegaiului, conservant pentru materialele celulozice , stabilizator pentru poliuretani și nailon , inhibitor de coroziune și aditiv pentru combustibil.
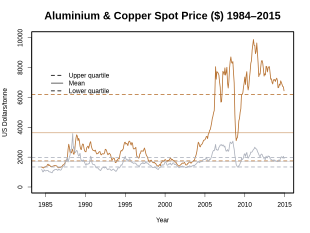
Dezvoltarea prețului
Cuprul este un metal relativ scump. Prețul său se bazează în mare măsură pe lume majore de mărfuri schimburile și bursele futures de mărfuri . London Metal Exchange (LME) este lider în comerțul cu cupru .
Prețul de pe piața mondială a cuprului este supus unor fluctuații puternice : a cunoscut una dintre cele mai mari fluctuații în 2008, când prețul cuprului de pe LME se tranzacționa încă la nivelul maxim intermediar de 8.940 USD / t la 2 iulie 2008 și la cel mai înalt nivel până pe 23 decembrie 2008 a scăzut cel mai scăzut nivel de 10 ani de 2.825 dolari. Ulterior, prețul cuprului s-a recuperat în mai puțin de 4 luni până la 15 aprilie 2009 la 4.860 USD / t. Prețul cuprului a atins maximul de 10 ani pe 14 februarie 2011, la 10.180 USD / t.
Din martie 2012 până în martie 2013, prețul cuprului a crescut la un nivel maxim la 2 aprilie 2012 la 8.619,75 USD și la 2 august 2012 la 7.288,25 USD. O gamă similară a fost găsită, de asemenea, din octombrie 2012 până în martie 2013 între 8.350 USD / t și 7.577 USD / t.
În august 2014, prețul pieței mondiale pentru cupru a fost de aproximativ 7.000 USD / t. Conform cursului de schimb din acel moment, acesta era de 5.931 EUR / t.
Prețul ridicat al cuprului determină, de asemenea, o creștere a furtului de obiecte care conțin cupru. Cablurile de împământare de pe căile ferate sunt afectate în mod special. De exemplu, Deutsche Bahn AG a suferit aproximativ 14 milioane de euro daune în 2015.
Unul dintre cele mai mari scandaluri financiare din istoria recentă este afacerea Sumitomo . S-a bazat pe comerțul cu cupru. Ca urmare a descoperirii, prețul cuprului a scăzut cu 27% în decurs de o zi, în 1996.
literatură
- Harry H. Binder: Lexiconul elementelor chimice - tabelul periodic în fapte, cifre și date. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3 .
- JW Howard: Povestea cuprului . În: Journal of Chemical Education . bandă 6 , nr. 3 , 1929, pp. 413-431 , doi : 10.1021 / ed006p413 ( PDF ).
Link-uri web
- Atlas mineral: cupru (date), atlas mineral: portret mineral / cupru (istoric, topire etc.)
- deutschlandfunk.de , Das Feature , 18 iulie 2017, Michael Faulmüller: Cupru - Element de discordie: O poveste de luptă eternă
- kupfer-institut.de ( Institutul German al Cuprului DKI)
- London Metal Exchange , lme.com: Prețul cuprului
Observații
- ↑ Valorile proprietăților (caseta de informații) sunt preluate de pe www.webelements.com (cupru) , dacă nu se specifică altfel .
Dovezi individuale
- ↑ a b Harry H. Binder: Lexiconul elementelor chimice. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3 .
- ↑ CIAAW, Standard Atomic Weights Revised 2013 .
- ↑ a b c d e Intrare pe cupru în Kramida, A., Ralchenko, Yu., Reader, J. și NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Ed.: NIST , Gaithersburg, MD. doi : 10.18434 / T4W30F ( https://physics.nist.gov/asd ). Adus la 11 iunie 2020.
- ↑ a b c d e Intrare pe cupru la WebElements, https://www.webelements.com , accesat pe 11 iunie 2020.
- ^ NN Greenwood, A. Earnshaw: Chimia elementelor. Prima ediție. VCH, Weinheim 1988, ISBN 3-527-26169-9 , p. 1509.
- ↑ Robert C. Weast (ed.): Manualul de chimie și fizică al CRC . CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9 , pp. E-129 până la E-145. Valorile acolo se bazează pe g / mol și sunt date în unități cgs. Valoarea dată aici este valoarea SI calculată din aceasta, fără o unitate de măsură.
- ↑ a b Yiming Zhang, Julian RG Evans, Shoufeng Yang: Valori corectate pentru punctele de fierbere și entalpiile de vaporizare a elementelor din manuale. În: Journal of Chemical & Engineering Data. 56, 2011, pp. 328-337, doi: 10.1021 / je1011086 .
- ^ A. Lossin: Cupru. În: Enciclopedia lui Ullmann de chimie industrială. Wiley-VCH Verlag, Weinheim 2005, doi : 10.1002 / 14356007.a07_471 .
- ↑ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Manual de fizică experimentală. Volumul 6: Solid. Ediția a II-a. Walter de Gruyter, 2005, ISBN 3-11-017485-5 , p. 361.
- ^ Buildingmaterials.de: Copper ( Memento din 15 noiembrie 2009 în Arhiva Internet )
- ^ Colecția de materiale de construcție a Facultății de Arhitectură de la Universitatea Tehnică din München: Metale - Cupru .
- ↑ Glyconet ( pagina nu mai este disponibilă , căutați în arhivele web ) Informații: linkul a fost marcat automat ca defect. Vă rugăm să verificați linkul conform instrucțiunilor și apoi să eliminați această notificare .
- ↑ a b c intrare pe cupru , în baza de date a substanței GESTIS IFA , accesat la 25 aprilie 2017. (JavaScript este necesar)
- ↑ Fondul elvețian de asigurare a accidentelor (Suva): valori limită - valorile actuale MAK și BAT (căutare cupru și compușii anorganici ai acestuia ), accesat la 4 martie 2020.
- ^ Wilhelm Hassenstein: Cartea focurilor de artificii din 1420. 600 de ani de arme pulverulente germane și fabricarea de arme. Reimprimarea primei ediții din 1529 cu traducere în limba germană standard și explicații, München 1941, p. 104.
- ↑ Pe bare de piele de bou, distribuția lor și comerțul cu cupru din epoca bronzului, vezi: Serena Sabatini: Revizitarea lingourilor din piele de ox din epoca bronzului târziu. Semnificații, întrebări și perspective. În: Ole Christian Aslaksen (Ed.): Perspective locale și globale asupra mobilității în Marea Mediterană de Est (= Lucrări și monografii de la Institutul Norvegian de la Atena, Volumul 5). The Norwegian Institute at Athens, Athens 2016, ISBN 978-960-85145-5-3 , pp. 15-62.
- ↑ Sungmin Hong, Jean-Pierre Candelone, Clair C. Patterson, Claude F. Boutron: Istoria poluării antice prin topirea cuprului în timpul timpurilor romane și medievale înregistrate în gheața din Groenlanda. În: Știință . Volumul 272, nr. 5259, 1996, pp. 246-249 (247, Fig. 1 și 2; 248, Tab. 1)
- ↑ Lista IMA / CNMNC a denumirilor minerale; Iulie 2019 (PDF 1,67 MB; cupru vezi p. 44)
- ↑ Lista de nume minerale IMA / CNMNC - cupru (engleză, PDF 1,8 MB, p. 64)
- ↑ Webmineral - Minerale aranjate de clasificarea New Dana. 01/01/01 Grupa aur
- ^ Cupru . În: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Eds.): Manual de Mineralogie, Mineralogical Society of America . 2001 ( handbookofmineralogy.org [PDF; 58 kB ; accesat la 22 ianuarie 2018]).
- ^ Atlas mineral: cupru
- ↑ Webmineral - Specii minerale sortate după elementul Cu (Cupru ).
- ↑ German Copper Institute - Disponibilitatea cuprului
- ↑ a b Lista localităților pentru cuprul solid din Mineralienatlas și Mindat
- ↑ Springer: Kupferberg, Paul Zsolnay-Verlag, Viena, 2019.
- ↑ Patrimoniul Mondial Cornish Miniere ( amintirea originalului din 17 februarie 2011 în Internet Archive ) Info: Arhiva link - ul a fost introdus în mod automat și nu a fost încă verificată. Vă rugăm să verificați linkul original și arhivă conform instrucțiunilor și apoi eliminați această notificare. .
- ↑ ICSG (Ed.): World Copper Fact Book 2020 .
- ↑ United States Geological Survey: World Mine Production and Reserves
- ↑ Pagina nu mai este disponibilă , căutați în arhivele web: cupru și produse realizate din acesta .
- ↑ TN Lung: Istoria cementării cuprului pe fier - Primul proces hidrometalurgic din lume din China medievală. În: Hidrometalurgie . Volumul 17, numărul 1, noiembrie 1986, pp. 113-129; doi: 10.1016 / 0304-386X (86) 90025-3 .
- ^ Ralph WG Wyckoff: Structuri de cristal . Ediția a II-a. bandă 1 . John Wiley & Sons, New York, Londra, Sydney 1963, pp. 3 (în anexă ).
- ^ Hugo Strunz , Ernest H. Nickel : Mese mineralogice Strunz. Sistem de clasificare a mineralelor chimico-structurale . Ediția a IX-a. E. Schweizerbart'sche Verlagbuchhandlung (Nägele și Obermiller), Stuttgart 2001, ISBN 3-510-65188-X , p. 34 .
- ↑ H. Keller, K. Eickhoff: Kuper and Copper Alloys, Springer-Verlag 2013, 54 de pagini, pagina 7
- ↑ George L. Trigg, Edmund H. Immergut: Enciclopedia fizicii aplicate , Volumul 4: Combustion to Diamagnetism. VCH Publishers, 1992, ISBN 978-3-527-28126-8 , pp. 267-272 (accesat la 2 mai 2011).
- ^ Architecture - German Copper Institute. Adus la 12 iulie 2021 (germană).
- ^ William Chambers, Robert Chambers: Chambers's Information for the People , 5. Ediție, volumul L, W. & R. Chambers, 1884, ISBN 978-0-665-46912-1 , p. 312.
- ^ Coroziune galvanică . În: Medici coroziune . Adus pe 29 aprilie 2011.
- ^ Universitatea din Siegen: Reacția metalelor cu acidul clorhidric .
- ↑ Fapte despre acest subiect - acid sulfuric ( Memento din 8 martie 2001 în Arhiva Internet )
- ^ Universitatea din Siegen: Reacția metalelor cu acidul azotic .
- ↑ chimia eLexiconului: clorură de cupru .
- ↑ Denise Herzog: Importanța cuprului în corpul uman: o scurtă prezentare generală . În: Revista elvețiană de medicină nutrițională . Nu. 1/10 .
- ↑ Jens Oliver Bonnet: Cupru împotriva germenilor: Așteptările au fost depășite. Asklepios Kliniken Hamburg GmbH, comunicat de presă din 16 iunie 2009 de la Informationsdienst Wissenschaft (idw-online.de), accesat la 15 septembrie 2015.
- ↑ Germkiller cupru - subiect de „știut la zi: puterea piraților celulari” .
- ↑ A sosit în practica clinică de zi cu zi? Materiale de construcție antimicrobiene pe bază de cupru solid , pe krankenhaushygiene.de
- ↑ https://www.amcopper.com/
- ↑ Salima Mathews, Michael Hans, Frank Mücklich, Marc Solioz: Uciderea prin contact a bacteriilor pe cupru este suprimată dacă contactul bacterian-metalic este prevenit și este indus pe fier de către ionii de cupru . În: Microbiologie aplicată și de mediu . bandă 79 , nr. 8 aprilie 2013.
- ↑ A. Ala, AP Walker, K. Ashkan, JS Dooley, ML Schilsky: Boala Wilson. În: The Lancet . Volumul 369, numărul 9559, februarie 2007, pp. 397-408, doi: 10.1016 / S0140-6736 (07) 60196-2 . PMID 17276780 .
- ^ SL Warnes, CW Keevil: Inactivarea norovirusului pe suprafețele uscate din aliaj de cupru. În: PLoS One. 8 (9), 2013, e75017. PMID 24040380 , PMC 3767632 (text complet gratuit, PDF).
- ↑ ratschlag24.com: Sârmă de cupru împotriva ciumei melcilor. ( Memento din 11 aprilie 2013 în arhiva web archive.today ) 17 martie 2008.
- ↑ sat1.de: difuzat 24: inteligent! - Carte de cunoștințe ( Memento din 26 mai 2011 în Arhiva Internet ).
- ↑ med.de: Intrare pe cupru , accesată la 23 februarie 2013.
- ↑ a b Manual Merck: Cupru .
- ↑ JF Mercer: sindromul Menkes și modele animale. În: Jurnalul american de nutriție clinică. Volumul 67, numărul 5 Suppl, mai 1998, pp. 1022S-1028S. PMID 9587146 . (Revizuire).
- ↑ S. Lutsenko, NL Barnes și colab.: Funcția și reglarea ATPazelor care transportă cuprul uman. În: Recenzii fiziologice . Volumul 87, numărul 3, iulie 2007, pp. 1011-1046, doi: 10.1152 / physrev.00004.2006 . PMID 17615395 . (Revizuire).
- ↑ TA Bayer: Cu dietetic stabilizează activitatea superoxidului dismutazei cerebrale 1 și reduce producția de amiloid Aβ la șoarecii transgenici APP23. În: Proceedings of the National Academy of Sciences. 100, 2003, pp. 14187-14192, doi: 10.1073 / pnas.2332818100 .
- ↑ Holger Kessler, Frank-Gerald Pajonk , Daniela Bach, Thomas Schneider-Axmann, Peter Falkai, Wolfgang Herrmann, Gerd Multhaup, Jens Wiltfang, Stephanie Schäfer, Oliver Wirths, Thomas A. Bayer: Efectul aportului de cupru asupra parametrilor LCR la pacienții cu boala Alzheimer ușoară: o fază pilot, 2 studii clinice. În: Journal of Neural Transmission. 115, 2008, pp. 1651-1659, doi: 10.1007 / s00702-008-0136-2 .
- ^ NG Faux, CW Ritchie, A. Gunn, A. Rembach, A. Tsatsanis, J. Bedo, J. Harrison, L. Lannfelt, K. Blennow, H. Zetterberg, M. Ingelsson, CL Masters, RE Tanzi, JL Cummings, CM Herd, AI Bush: PBT2 îmbunătățește rapid cunoașterea în boala Alzheimer: analize suplimentare de fază II. În: Jurnalul bolii Alzheimer: JAD. Volumul 20, numărul 2, 2010, pp. 509-516, doi: 10.3233 / JAD-2010-1390 . PMID 20164561 .
- ↑ I. Singh, AP Sagare, M. Coma, D. Perlmutter, R. Gelein, RD Bell, RJ Deane, E. Zhong, M. Parisi, J. Ciszewski, RT Kasper, R. Deane: Nivelurile scăzute de cupru perturbă homeostazia creierului amiloid-β prin modificarea producției și a clearance-ului acestuia. În: Proceedings of the National Academy of Sciences. S., doi: 10.1073 / pnas.1302212110 .
- ↑ Deutsches Kupferinstitut: Cupru și aplicațiile sale ( amintirea originalului din 16 iulie 2012 în arhiva web archive.today ) Info: Arhiva link - ul a fost introdus în mod automat și nu a fost încă verificată. Vă rugăm să verificați linkul original și arhivă conform instrucțiunilor și apoi eliminați această notificare. .
- ↑ Aliaje de cupru. Adus la 12 iulie 2021 .
- ^ R. Neeb: polarografie inversă și voltametrie. Akademie-Verlag, Berlin 1969, pp. 185–188.
- ↑ a b Georg Brauer (Ed.), Cu colaborarea Marianne Baudler și alții: Manual de chimie anorganică preparativă. Ediția a treia, revizuită. Volumul II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , p. 979.
- ↑ a b c d Inventarul național al poluanților: cupru și compuși
- ↑ Georg Brauer (Ed.), Cu colaborarea Marianne Baudler și alții: Manual de chimie anorganică preparativă. Ediția a treia, revizuită. Volumul II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , p. 973.
- ↑ Lider în comerțul cu cupru: London Metal Exchange - LME Copper . Adus la 15 martie 2013.
- ↑ a b c evoluția prețului cuprului la London Metal Exchange în perioada 7.doi.2008-4.cincisprezece.2009 ( Memento din originalul de la 12 august 2014 în Internet Arhiva ) Info: Arhiva link a fost introdus automat și încă nu a fost verificat. Vă rugăm să verificați linkul original și arhivă conform instrucțiunilor și apoi eliminați această notificare. Sursa: baza de date Handelsblatt. Adus la 15 martie 2013.
- ↑ Cel mai mare preț pentru cupru la London Metal Exchange din ultimii 10 ani pe 14 februarie 2011 Sursa: Handelsblatt. Adus la 15 martie 2013.
- ↑ Evoluția prețului cuprului la London Metal Exchange în ultimele 12 luni Sursa: Handelsblatt. Adus la 15 martie 2013.
- ↑ Evoluția prețului la cupru la London Metal Exchange în ultimele 6 luni Sursa: Handelsblatt. Adus la 15 martie 2013.
- ↑ prețul curent pentru cupru la London Metal Exchange ( amintirea originalului din 12 august 2014 în Internet Archive ) Info: Arhiva link - ul a fost introdus în mod automat și nu a fost încă verificată. Vă rugăm să verificați linkul original și arhivă conform instrucțiunilor și apoi eliminați această notificare. Sursa: Handelsblatt.
- ↑ Această cifră a fost determinată cu șablonul: Rata de schimb .
- ^ Furtul de metale neferoase la Deutsche Bahn. (Nu mai este disponibil online.) Biroul de presă Deutsche Bahn, arhivat din original la 23 decembrie 2016 ; accesat pe 22 decembrie 2016 .