Hepatita C.
| Clasificare conform ICD-10 | |
|---|---|
| B17.1 | Hepatita virală acută C |
| B18.2 | Hepatita virală cronică C. |
| ICD-10 online (versiunea OMS 2019) | |
Hepatita C este de virusul hepatitei C infectie bolii cauzate la om. Se caracterizează printr-o rată ridicată de cronificare (până la 80%), care, în curs, poate duce la leziuni hepatice severe, cum ar fi ciroză și carcinom hepatocelular . Se transmite parenteral prin sânge. Tratamentul hepatitei cronice C, adică eliminarea completă a virusului, este posibil în până la 99% din cazuri prin utilizarea substanțelor care au efecte antivirale directe. Un vaccin împotriva hepatitei C nu există încă.
În 2020, Harvey J. Alter , Michael Houghton și Charles M. Rice au primit Premiul Nobel pentru fiziologie sau medicină pentru descoperirea virusului .
Patogen
Virusul hepatitei C (VHC) a fost identificat pentru prima dată în 1989 , cu ajutorul ingineriei genetice (detectarea materialului genetic) (anterior hepatita non-A non-B). Este un virus ARN monocatenar (+) învelit de 45 nm și aparține genului Hepacivirus din familia Flaviviridae . Există șapte genotipuri și 67 de subtipuri . De exemplu, genotipurile 1, 2 și 3 se găsesc predominant în Europa și SUA și de tip 4. În Africa. Până în prezent, se presupunea că oamenii sunt singurele gazde naturale ale virusului hepatitei C. În timp ce caută originea agentului patogen la rozătoare, o echipă internațională de oameni de știință a găsit multe variante ale virusurilor asemănătoare VHC. Anticorpii împotriva agentului patogen ar putea fi detectați la lilieci. Prin urmare, acum se crede că această familie de viruși a evoluat inițial la rozătoare.
transmisie
În aproximativ 30% dintre boli, calea infecției nu mai poate fi urmărită retrospectiv . Astăzi, există un risc crescut de infecție pentru utilizatorii de droguri, cum ar fi heroina, care consumă intravenos și împart aceleași seringi cu alți utilizatori, precum și pentru persoanele care consumă medicamente nazale prin partajarea (adulmecarea) tuburilor. De asemenea, tatuajele și piercingurile folosesc instrumente contaminate este un factor de risc. Căile frecvente de infecție sunt leziunile cu instrumente ascuțite și ascuțite ( leziuni cu ace (NSV)) cu transmitere simultană a sângelui contaminat. Riscul de infecție după INS cu o persoană cunoscută cu indice pozitiv este dat în literatura de specialitate între 3 și 10%. Astfel, este mai mare decât riscul mediu de transmitere a HIV , dar, la fel ca în cazul HIV, pare a fi foarte dependent de viremia persoanei indexate.
Au fost, de asemenea, afectați pacienții cu hemofilie care depindeau de sânge / plasmă donator sau de preparate de coagulare din sânge uman, de exemplu, pentru intervenții chirurgicale. În acea perioadă, hepatita C și B erau adesea trecute neobservate acestor pacienți. Odată cu introducerea procedurilor moderne de testare, cu ajutorul cărora astăzi pot fi identificați peste 99% din donatorii de hepatită C-pozitivi, există doar un risc minim de infecție prin transfer de sânge. O altă cale posibilă de infecție este transplantul de ficat.
Transmiterea sexuală a hepatitei C este rară. Deoarece virusul este transmis prin sânge, practicile sexuale care prezintă un risc mai mare de leziuni ale mucoasei, cum ar fi actul sexual neprotejat , prezintă un risc mai mare. Frecvența transmiterii virusului de la mama gravidă la copilul nenăscut este estimată a fi mai mică de 5% dacă nașterea este simplă. În cazul unei co-infecții cu virusul HI , transmisia poate crește până la 14%.
Perioada de incubație este cuprinsă între 2 și 26 de săptămâni (6 luni).
Epidemiologie
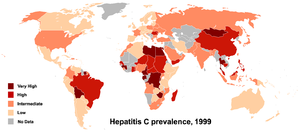
Prevalența este de 2,6% la nivel mondial, 0,5% în Germania și 5,0% și mai mult în zonele de mare risc ale lumii (zonele roșu închis pe hartă) - până la 48% în Mongolia.
Institutul Robert Koch (RKI) publică cifre privind situația epidemiologică a hepatitei C în fiecare an . Pentru anul 2005, aceasta se ridică la 8.308 diagnostice inițiale înregistrate în Germania. Puțin mai mult de 50% dintre acestea au fost determinate de diagnostic de laborator și nu au avut un tablou clinic tipic. Diagnosticul de laborator nu poate face diferența între infecțiile VHC acute și de lungă durată.
Aproximativ 170 de milioane de oameni din întreaga lume sunt infectați cu virusul HC, în Germania sunt afectate 400.000 până la 500.000 de persoane. Principalul grup de risc pentru infecția cu VHC sunt utilizatorii intravenoși de droguri injectabile, dintre care 60 până la 90 la sută sunt purtători de VHC. În schimb, într-un studiu din SUA, 48,4% din totalul persoanelor pozitive anti-VHC cu vârste cuprinse între 20 și 59 de ani au consumat droguri intravenoase.
Numărul de cazuri raportate la RKI pentru Germania sa dezvoltat după cum urmează din anul 2000:
| an | numere de caz raportate |
|---|---|
| 2000 | 5091 |
| 2001 | 4350 |
| 2002 | 6698 |
| 2003 | 8762 |
| 2004 | 8955 |
| 2005 | 8357 |
| 2006 | 7560 |
| 2007 | 6867 |
| 2008 | 6223 |
| 2009 | 5431 |
| 2010 | 4998 |
| 2011 | 5056 |
| 2012 | 4996 |
| 2013 | 5168 |
| 2014 | 5825 |
| 2015 | 4872 |
| 2016 | 4422 |
| 2017 | 4733 |
| 2018 | 5899 |
| 2019 | 6633 |
Diagnostic
Diagnosticul se bazează pe detectarea anticorpilor specifici virusului împotriva proteinelor structurale și nestructurale utilizând imunoanalize enzimatice și imunobloti, precum și pe detectarea unor părți ale genomului virusului (HCV-ARN) utilizând reacția în lanț a polimerazei ( RT-PCR ). Dacă există un test anticorp cu siguranță pozitiv și o PCR negativă multiplă la un interval de cel puțin trei luni, se poate presupune că infecția s-a vindecat mai devreme. O biopsie hepatică sau o sonografie hepatică pot face afirmații fiabile despre stadiul bolii (stadiul afectării țesuturilor). Spre deosebire de alte hepatite, nivelurile transaminazelor din sânge (GGT, GPT , GOT ) sunt adesea independente de gravitatea sau stadiul bolii și, prin urmare, nu sunt un marker de încredere pentru evoluția reală a bolii.
curs
Hepatita C nu este adesea diagnosticată în faza acută datorită cursului în mare parte fără simptome sau cu simptome scăzute (în 85% din cazuri). Posibile reclamații după o perioadă de incubație de 20 până la 60 de zile sunt oboseala, epuizarea, pierderea poftei de mâncare, dureri articulare, senzație de presiune sau tensiune la nivelul abdomenului superior drept și posibil pierderea în greutate. Icterul se dezvoltă la unii oameni ; urina poate fi foarte întunecat și scaun de culoare lut. În multe cazuri, persoana afectată nu percepe deloc boala sau o percepe doar ca pe o presupusă infecție asemănătoare gripei . Cu toate acestea, faza acută se transformă într-o formă cronică în mai mult de 70% din cazuri. Datorită variabilității mari a virusului și a suprimării specifice specifice a unui răspuns adecvat al celulelor T, virusul se reproduce constant și cauzează astfel o infecție cronică.
Dacă infecția rămâne netratată, aceasta va duce la ciroză hepatică la aproximativ un sfert din pacienți pe termen lung, după aproximativ 20 de ani . Există, de asemenea, un risc crescut de carcinom cu celule hepatice .
În cursul unei infecții cronice cu VHC, pot apărea în continuare boli mediate în special de anticorpi. Acestea includ crioglobulinemia (deosebit de frecventă în genotipul 2), sindromul Sjogren , panarterita nodoză și glomerulonefrita cu complex imunitar . În legătura cauzală stabilită cu infecția cu VHC, bolile extrahepatice descrise sunt rezistența la insulină / diabetul zaharat, crioglobulemia vasculită, bolile limfoproliferative, performanța afectată (oboseală, oboseală) și simptomele depresive.
terapie
Terapie standard și algoritmi de terapie
Conform terapiei standard aplicate în 2009, hepatita C acută a fost tratată virostatic cu PEG-interferon alfa 2-b împreună cu ribavirină după o perioadă de așteptare de trei luni și rezultat persistent pozitiv al ARN-VHC, similar hepatitei cronice C. Alternativ, ar putea fi luată în considerare și administrarea imediată de interferon singur pe o perioadă de șase luni.
Ca un tratament standard pentru VHC genotipurile 1 și 4 a fost 2015 combinație de sofosbuvir și Ledipasvir ( Harvoni ® ), pentru genotipuri HCV 2 și 3, o combinație de sofosbuvir și ribavirină pentru genotipurile HCV 5 și 6, o combinație de Ledipasvir și sofosbuvir și ribavirină , sau ca alternativă pentru VHC genotipul 3, se recomandă o combinație de daclatasvir și sofosbuvir .
„Recomandarea actuală pentru terapia hepatitei cronice C” a Societății Germane de Gastroenterologie, Boli Digestive și Metabolice (DGVS) numește „medicamente aprobate” pentru terapia hepatitei C (status: 7/2015):
- terapie convențională:
- Peginterferon α pentru inițială și re-terapie pentru toate genotipurile
- Ribavirina ca terapie combinată pentru inițială și re-terapie pentru toate genotipurile
- Inhibitori de protează:
- Simeprevir ( Olysio ® de la Janssen Pharmaceutica ) ca terapie combinată pentru inițială și re-terapie pentru genotipurile 1 și 4
- Paritaprevir (companie farmaceutică: AbbVie ) ca terapie combinată pentru inițială și re-terapie pentru genotipurile 1 și 4
- Asunaprevir , ciluprevir , danoprevir , glecaprevir , grazoprevir , narlaprevir , sovaprevir , vaniprevir , voxilaprevir
- nu mai este recomandat ca terapie standard:
- Telaprevir (UE: Incivo ® , Titularul autorizației de punere pe piață : Janssen-Cilag , SUA: Incivek ® , Titularul autorizației de punere pe piață : Vertex Pharmaceuticals ) ca terapie combinată pentru inițială și re-terapie pentru genotipul 1
- Boceprevir ( Victrelis ® , companie farmaceutică: MSD Sharp & Dohme ) ca terapie combinată pentru inițială și re-terapie pentru genotipul 1
- Faldaprevir , vedroprevir
- Inhibitori NS5A:
- Daclatasvir ( Daklinza ® , companie farmaceutică: Bristol-Myers Squibb ) ca terapie combinată pentru inițială și re-terapie pentru genotipurile 1 - 6
- Ledipasvir (companie farmaceutică: Gilead Sciences ) ca terapie combinată pentru inițială și re-terapie pentru genotipurile 1, 3, 4 și 6
- Ombitasvir (companie farmaceutică: AbbVie) ca terapie combinată pentru inițială și re-terapie pentru genotipurile 1 și 4
- Elbasvir , Odalasvir , Pibrentasvir , Ravidasvir , Ruzasvir , Samatasvir , Velpatasvir
- Inhibitori non-nucleozidici polimerazici (NS5B):
- Dasabuvir (UE: Exviera ® , titularul autorizației de punere pe piață : AbbVie) ca terapie combinată pentru inițială și re-terapie pentru genotipul 1
- Beclabuvir , Deleobuvir , Filibuvir , Setrobuvir , Radalbuvir , Uprifosbuvir
- Inhibitori ai nucleozelor (t) polimerazei idice (NS5B):
- Sofosbuvir ( Sovaldi ® , companie farmaceutică: Gilead Sciences) ca terapie combinată pentru inițială și re-terapie pentru toate genotipurile
Sofosbuvir este al treilea ingredient activ DAA (denumit „agent antiviral direct”, „agent antiviral cu acțiune directă”, „substanță antivirală directă” sau „medicament antiviral cu acțiune directă”) care intervine în replicarea virusului, dar prima polimerază -Inhibitor.
La începutul anului 2015, DGVS a publicat un addendum la orientarea sa din 2014, care recomandă terapia combinată fără interferon cu sofosbuvir și ribavirină pentru terapia inițială în genotipul 2.
Ledipasvirul din grupul inhibitorilor NS5A a fost aprobat în UE în 2014 ca produs combinat cu sofosbuvir ( Harvoni ® ).
O terapie combinată aprobată de la AbbVie ( Viekirax ® ) constă din ombitasvir, paritaprevir și ritonavir .
Fostă terapie standard
Tratamentul standard (starea 2009) a constat într-o terapie combinată cu interferon α pegilat (peginterferon alfa-2a sau peginterferon alfa-2b) și ribavirină antivirală pentru o perioadă de 24 până la 48, rareori 72 de săptămâni. Peg-interferonul se injectează sub piele o dată pe săptămână, ribavirina se administrează zilnic sub formă de tablete (uneori și sub formă lichidă pentru copii).
Scopul tratamentului este ca șase luni după terminarea terapiei să nu poată fi detectat niciun virus (VHC-ARN negativ). Dacă se atinge acest punct, pacientul este considerat vindecat. Recidivele ulterioare sunt foarte rare.
În funcție de genotipul virusului prezent la pacient, există o șansă de 50 până la 80% de a elimina definitiv virusul cu această terapie. Cu genotipurile 2 și 3, probabilitatea de succes este semnificativ mai mare decât cu genotipul 1. Alți factori importanți pentru o terapie de succes sunt vârsta, sexul, încărcătura virală , durata bolii, greutatea corporală și gradul de afectare a ficatului. Boli suplimentare, cum ar fi infecția cu HIV sau hepatita B, pot îngreuna terapia.
Între timp, durata terapiei nu este ajustată numai în funcție de genotip, ci și în funcție de cât de repede sau încet scade cantitatea de virus în primele 4, 12 și, eventual, 24 de săptămâni.
Cu tratamentul cu hepatita C, sunt de așteptat numeroase efecte secundare, care variază în severitate în funcție de pacient. (Peg) -Interferonul α poate duce, printre altele, la simptome asemănătoare gripei (febră, frisoane), oboseală, ușoară cădere a părului, funcționarea defectuoasă a glandei tiroide și efecte secundare psihologice, cum ar fi depresia , agresivitatea sau anxietatea. Dacă pacienții au deja antecedente de depresie, se poate administra un antidepresiv în anumite cazuri înainte de a începe terapia cu interferon . Cel mai frecvent efect secundar al ribavirinei este scăderea globulelor roșii ( hemoliză ); acest lucru poate duce la reducerea dozei de ribavirină și, în cazuri severe, tratamentul este întrerupt prematur. Deoarece o cantitate suficientă de ribavirină este importantă pentru șansele de recuperare, se încearcă evitarea reducerii dozelor pe cât posibil.
Decizia pentru sau împotriva terapiei se ia individual. Evoluția respectivă a bolii, eventualele contraindicații și oportunitățile de tratament probabile, dar și situația de viață a persoanei în cauză, sunt importante pentru decizie. Tratamentul trebuie efectuat și monitorizat de un medic cu experiență în terapie.
Un nou studiu a arătat că pacienții cu hepatită C acută pot beneficia dacă începutul tratamentului este întârziat cu câteva săptămâni. O cincime dintre pacienți s-au putut vindeca spontan, după care terapia nu a mai fost necesară.
Droguri noi
Pe lângă noii interferoni și înlocuitori ai ribavirinei, se efectuează cercetări și asupra mijloacelor care împiedică înmulțirea directă a virusului ( inhibitori de protează și polimerază). În 2011, inhibitorii de protează telaprevir și boceprevir au fost aprobați în SUA, UE și Japonia. Atât boceprevirul, cât și telaprevirul trebuie combinate cu interferon și ribavirină. Ambele substanțe sunt aprobate numai pentru genotipul 1 al virusului hepatitei C. Inhibitorii de protează și polimerază, ca substanțe individuale, reduc semnificativ încărcătura virală (la valori sub 600.000 UI / ml), dar provoacă rapid rezistență, ceea ce crește din nou cantitatea de virus. Terapiile triple cu telaprevir sau boceprevir sunt semnificativ mai eficiente în genotipul 1, dar trebuie luate în considerare efectele secundare și interacțiunile cu alte medicamente. Telaprevir și boceprevir pot agrava anemia. Cu telaprevir, erupțiile cutanate și mâncărimea în zona anală sunt observate mai des. Tulburările gustative (disgeuzia) pot apărea mai des cu boceprevir.
În plus față de substanțele antivirale în combinație cu interferon și ribavirină, se efectuează și cercetări în terapiile fără interferon împotriva hepatitei C. În aprilie 2011, la Congresul hepatic EASL, au fost raportate cure fără interferon în condiții controlate pentru prima. timp: 4 din 11 pacienți cu hepatită C cu genotipul 1 au fost vindecați prin tratament fără interferon cu asunaprevir și daclatasvir. Daclatasvir și alții sunt deosebit de convingători datorită terapiei relativ scurte necesare, deoarece sarcina virală este redusă din prima zi. Sunt cercetate alte terapii combinate fără interferon. O terapie combinată de 12 săptămâni a GS-7977 (PSI-7977) cu ribavirină a reușit să vindece 10 din 10 pacienți cu hepatită C cu genotipurile 2 și 3, dar această dublă combinație a fost suficientă la pacienții cu genotip 1 VHC pretratați anterior fără succes („ zero -Răspuns "fără răspuns virologic rapid și fără răspuns virologic timpuriu ) nu este eficient pentru vindecare.
O combinație de sofosbuvir și velpatasvir ( Epclusa ® ) a dus la o rată de vindecare de 99% într-un studiu.
prevenirea
Nu este aprobat niciun vaccin pentru imunizarea activă împotriva hepatitei C. Măsurile de protecție existente s-au limitat la prevenirea expunerii prin evitarea contactului sânge-sânge cu persoanele infectate, de exemplu, atunci când se iau medicamente intravenoase, toată lumea își folosește doar seringa și acul. Pentru a reduce tentația de a folosi seringile împreună, centrele de consiliere pentru droguri oferă gratuit seturi de injecție. Persoanele infectate ar trebui să învețe să fie atenți cu sângele ( ajutor SIDA ). Aceasta include în principal conștientizarea posibilului contact cu sângele și evitarea împărțirii foarfecelor de unghii, aparat de ras și periuțe de dinți cu persoanele neinfectate. În plus, barierele fluide, cum ar fi prezervativele și barajele dentare , ar trebui utilizate în timpul actului sexual .
Nu există profilaxie post- expunere după infecția cu hepatita C, așa cum se știe în hepatita B sau HIV. Dacă hepatita C este descoperită și tratată în primele șase luni după infecție, o terapie cu interferon de 24 de săptămâni poate duce la o vindecare în peste 90% din cazuri înainte ca boala să devină cronică.
Transmiterea virusurilor hepatitei C prin măsuri medicale
Transmiterea ca parte a tratamentului schistosomiazei
Între anii 1950 și 1980, autoritățile egiptene de sănătate s-au luptat împreună cu Organizația Mondială a Sănătății pentru a exista schistosomiază foarte comună cu campanii organizate în care s-a injectat emeticul tartru bolnav ( emeticul tartru ). Virusul hepatitei C a fost probabil infectat prin canule care nu au fost dezinfectate în mod adecvat. În examinările serologice ulterioare antigenele virusului ar putea fi detectate în 70-90% din toate cazurile de hepatită cronică, ciroză hepatică și carcinom cu celule hepatice. Numărul persoanelor afectate este estimat la șase milioane. Întrucât complicațiile menționate mai sus ale unei infecții cu virusul hepatitei C au apărut adesea abia după douăzeci de ani, infectiologii consideră că punctul culminant al epidemiei de boli hepatice din Egipt este încă în curs. Este probabil cel mai grav caz de agenți patogeni medicali ( iatrogeni ) din istorie.
Transmiterea ca parte a unei profilaxii imune anti-D
Profilaxia imunitară anti-D este menită să prevină o reacție de respingere împotriva unui făt rhesus pozitiv la o mamă căreia îi lipsește factorul Rh D (rhesus negativ) într-o a doua sarcină. La naștere, sângele copilului pătrunde întotdeauna în fluxul sanguin al mamei. Dacă femeia este resus negativă și copilul ei este resus pozitiv, femeia poate dezvolta anticorpi împotriva factorului resus, care îi este străin. Într-o altă sarcină cu un făt pozitiv la resus, anticorpii materni pot trece apoi prin placentă și pot duce la dizabilități la făt și chiar la moarte. Pentru a evita acest lucru, imunoglobulinele anti-D sunt injectate imediat după nașterea primului copil și a celui următor, protejând astfel frații ulteriori.
Germania
În RDG , profilaxia imună anti-D era cerută de lege. În 1978 și 1979, câteva mii de femei au primit imunoglobuline contaminate cu virusuri ale hepatitei C - în rapoartele de presă erau 6.700. Producătorul (BIBT Halle) și deținătorul brevetului de imunoprofilaxie GDR anti-D era deja conștient de contaminarea cu virusul hepatitei C a materiei prime (plasma sanguină) în 1978 înainte de producerea loturilor serice relevante. Donatorii de plasmă din sânge (materie primă de producție pentru imunoprofilaxie anti-D) au fost în tratament intern pentru hepatita acută non-A-non-B (virusul hepatitei C) și, prin urmare, era deja clar înainte de producerea serului anti-D că plasma sanguină donată de pacienții internați trebuia să fie contaminată cu virusul non-A-non-B (hepatita C). Prin urmare, nu a fost doar un scandal al drogurilor , ci și cea mai mare infracțiune împotriva drogurilor din RDG, așa cum este documentat în dosarele ședinței principale nepublicate a diviziei a 4-a penale a instanței de district Halle / Saale (dosarul numărul 4 BS 13/79 din 27 noiembrie 1979). Loturile contaminate cu virus au fost eliberate de către Institutul raional pentru donarea și transfuzia de sânge din districtul Halle (BIBT) și Institutul de control al statului pentru seruri și vaccinuri (sursă: dosare de investigație pentru dosarul nr. 4 BS 13/79). Victimele criminalității anti-D au fost inițial sprijinite în baza Legii RDG pentru prevenirea și controlul bolilor transmisibile la oameni (GüK). Guvernul federal din Germania reunificată a susținut atunci că despăgubirea era o chestiune de stat. Femeile afectate au fost considerate vaccinate și, prin urmare, au primit beneficii în temeiul Legii federale a bolilor . La 9 iunie 2000, Bundestag a adoptat legea anti-D-Aid , conform căreia femeile infectate, copiii lor infectați născuți după imunoprofilaxie și alte persoane de contact infectate au dreptul la tratament medical și ajutor financiar. Beneficiile de pensie sunt cuprinse între 271 și 1082 de euro pe lună (începând cu 2004); Au fost acceptate 2464 de cereri. Vârful plăților unice a fost atins în 2000 cu șapte milioane de euro; În plus, aproximativ două milioane de euro sunt plătiți anual în pensii, din care cel puțin jumătate este finanțat de guvernul federal. În 2001, Oficiul Federal de Audit a examinat punerea în aplicare a legii și a criticat gestionarea neconcordantă a cererilor în statele federale; el a sugerat o supraveghere federală mai strictă. În ceea ce privește numărul de persoane afectate, acesta este - după scandalul Contergan - cel mai mare scandal farmaceutic din istoria postbelică germană.
Pentru cei infectați cu HIV în așa-numitul scandal al sângelui din anii 1990, 90 la sută din cazuri au fost co-infectați cu produse din sânge contaminate cu virusul hepatitei C. Acest scandal de sânge a afectat, de asemenea, aproximativ 1200 de pacienți hemofili care nu au fost co-infectați cu virusul HIV. La fel ca infecția cu HIV, aceste infecții ar fi putut fi prevenite prin inactivarea adecvată a virusului a preparatelor de coagulare. Până în prezent (din vara anului 2019) nu a existat nicio compensație pentru acest scandal de sânge al hepatitei C.
Irlanda
În Irlanda, donațiile de sânge au fost testate pentru anticorpi împotriva virusului hepatitei C din octombrie 1991. Un studiu regional a constatat că 13 din 15 femei infectate erau rhesus negative (trei s-ar fi așteptat); în același timp, erau mult mai în vârstă decât donatorul mediu. Doisprezece dintre aceste femei primiseră imunoprofilaxie anti-D în 1977. Această descoperire a declanșat o criză de încredere în Consiliul serviciului irlandez de transfuzie de sânge . În 1996 a fost înființată o comisie națională de anchetă. Peste 62.000 de femei care au primit imunoprofilaxie între 1970 și 1994 au fost testate și au constatat că loturile de imunoglobuline anti-D utilizate în 1977 și 1978 au fost contaminate cu virusul hepatitei C. Comisia a concluzionat că plasma sanguină a unei singure persoane contaminate a provocat contaminarea. În 1997 a fost înființat un tribunal pentru a se pronunța asupra cererilor de despăgubire. Din 1.871 de cereri, 1.042 (începând cu noiembrie 1998) au fost recunoscute drept eligibile și s-au plătit compensații în valoare totală de 219 milioane dolari. Aceasta echivalează cu o compensație medie de 210.173 dolari pe caz.
155 de femei au fost urmărite la 22 de ani după infecția inițială. Cele mai frecvente simptome raportate au fost oboseala și durerile articulare; 77 la sută dintre femei au avut, de asemenea, simptome semnificative din punct de vedere clinic ale anxietății. Infecția cu hepatită C a putut fi detectată doar cu PCR la 87 de femei ; celelalte par să fi eliminat virusul în mod spontan; cu toate acestea, aproape jumătate dintre aceștia au prezentat încă anticorpi. În mod surprinzător, fiecare a cincea femeie din acest grup avea hepatită. O biopsie hepatică a fost, de asemenea, efectuată la 27 (40%) dintre pacienții cu PCR-negativi, care au relevat modificări inflamatorii minime, cum ar fi inflamația ușoară și fibroza minimă. Patru (14,8%) persoane au prezentat rezultate histologice normale ale ficatului, 20 (74%) persoane au avut inflamație ușoară și trei (11,1%) persoane au avut afecțiuni hepatice moderate până la severe. Doar 3,4% dintre femeile cu viruși detectabili au avut hepatită. Încărcătura virală nu pare să reflecte severitatea simptomelor clinice. În nici un caz nu a putut fi detectată ciroză sau carcinom hepatocelular . În general, acest studiu a arătat că, într-o proporție surprinzător de mare de femei, corpul lor eliminase virusul și că boala nu tindea să se înrăutățească de-a lungul anilor. În ciuda evoluției favorabile a bolii observate aici, au existat simptome psihologice puternice de stres și o calitate slabă a vieții.
Transmiterea prin coagulanți de sânge
În Japonia, din octombrie 2002, aproximativ 240 de persoane au dat în judecată statul pentru infecție cu virusuri hepatitice C de la coagulanți din sânge, în special fibrinogen . Majoritatea bolnavilor primiseră produse din sânge în timpul nașterii. În ianuarie 2008, guvernul a încheiat procedura judiciară printr-o soluționare: pe această bază, parlamentul japonez a adoptat o lege pe 15 ianuarie care acorda victimelor despăgubiri între 12 și 40 de milioane de yeni (aproximativ 75.000 - 250.000 de euro). Aproximativ 1.000 de persoane au fost desemnate inițial drept eligibile. Primul ministru Yasuo Fukuda și-a cerut scuze față de cei afectați și și-a asumat responsabilitatea în numele statului. Fondul de compensare va fi asigurat cu 20 de miliarde de yeni, în care vor plăti și producătorii de produse din sânge contaminate. La 15 februarie 2008, Ministerul Sănătății a dezvăluit că se crede că numărul efectiv de persoane infectate este de 8.896. Până în prezent, doar aproximativ 40% dintre cei afectați au fost informați. În calitate de producători de produse din sânge contaminate, trei companii, Mitsubishi Tanabe Pharma Corp. precum și filiala sa Benesis Corp. și Nihon Pharmaceutical Co. numită. La Mitsubishi Tanabe este succesorul Green Cross Corp. pe care fibrinogenul le-a produs inițial. Crucea Verde a devenit faimoasă în Japonia deoarece un număr mare de oameni au dezvoltat SIDA după ce au vândut produse din sânge contaminate cu HIV .
Cel mai mare risc de infectare cu hepatita C a fost la primitorii de produse din sânge obținute din câteva mii de donații individuale, cum ar fi: B. Hemofili . Clarificarea circumstanțelor exacte ale așa-numitului „scandal al sângelui ”, în care a fost discutată în primul rând infecția cu produse din sânge contaminate cu HIV , continuă până în prezent.
Transmiterea prin seringi contaminate
Potrivit unui studiu realizat de Universitatea din Valencia, anestezistul Juan Maeso Vélez a infectat cel puțin 171 de pacienți cu hepatită C între 1994 și 1998 în două spitale din Valencia. Studiul, cu care a fost posibil să fie arestat Maeso ca singură sursă, a fost realizat ca parte a unui proces în 2000.
Potrivit rapoartelor de presă, mai multe persoane dintr-o clinică din Las Vegas s-au infectat cu virusuri ale hepatitei sau HIV prin seringi necurate . Din martie 2004, se spune că angajații din „Centrul de endoscopie din sudul Nevada” au folosit seringi de unică folosință și flacoane de injecție de mai multe ori conform instrucțiunilor directorului clinicii, astfel încât virusurile să poată fi transmise în acest mod. Scandalul a ieșit la iveală atunci când șase cazuri de hepatită C au fost raportate districtului responsabil în februarie 2008.
Aspecte de cost
O terapie de douăsprezece săptămâni cu cele mai eficiente tablete Sofosbuvir costă în jur de 43.562,52 euro în Germania începând cu 23 ianuarie 2015. Între timp, costul tratamentului a scăzut la 29.989,95 euro, ceea ce ar duce la un preț de 357,02 euro pe tabletă (începând din aprilie 2020). Producătorul Gilead a raportat vanzari la nivel mondial sofosbuvir de $ 5,7 la miliarde de euro în prima jumătate a anului 2014 . În Egipt, unde până la 22% din populație este infectată cu VHC, un acord cu Gilead ar oferi 150.000 de pacienți în stadiu critic sofosbuvir pentru 300 de dolari în loc de 84.000 de dolari pe care nu i-ar putea plăti niciodată. Costurile ridicate ale ultimei generații de medicamente sunt controversate și conduc la restricții din partea companiilor de asigurări atunci când vine vorba de rambursarea costurilor. Costurile opțiunilor de terapie anterioare, de ex. B. cu interferon + ribavirină + telaprevir sunt în funcție de durata terapiei antivirale între 7.800 euro și 35.000 euro per pacient.
Cerința de raportare
În Germania, fiecare hepatită acută virală (inclusiv hepatita acută C) trebuie raportată pe nume, în conformitate cu secțiunea 6 din Legea privind protecția împotriva infecțiilor (IfSG) . Aceasta privește suspiciunea unei boli, boala și decesul cauzat de această boală infecțioasă. În plus, orice dovadă a virusului hepatitei C trebuie raportată pe nume, în conformitate cu § 7 IfSG.
În Austria, după § 1 1 alin. Epidemics Act 1950 privind suspiciunea, boala și decesele cauzate de hepatita infecțioasă (hepatita A, B, C, D, E) , inclusiv hepatita C, cu notificare .
De asemenea , în Elveția , este supusă hepatitei C , cerința de raportare și că , după Legea Epidemiile (GPI) , în legătură cu Regulamentul epidemice și Anexa 1 din Regulamentul EDI privind raportarea observațiilor bolilor transmisibile și a omului . Criteriile de raportare pentru acest mesaj de către medici, spitale etc. sunt o constatare pozitivă de analiză de laborator și cererea de către medicul cantonal sau raportul medical cantonal , cazul. Laboratoarele trebuie să raporteze rezultate pozitive de laborator pentru virusul hepatitei C în conformitate cu apendicele 3 la ordonanța EDI menționată mai sus.
literatură
- H. Wedemeyer, M. Cornberg, MP Manns: interferoni PEG: Importanță pentru terapia hepatitelor virale B și C. În: Dtsch Med Wochenschr. 2001 1 iunie; 126 Suppl 1, pp. S68-S75, PMID 11450618
- E. Herrmann, C. Sarrazin: virusul hepatitei C - cinetica virusului și mecanisme de rezistență. În: Z Gastroenterol. 1998; 36, pp. 997-1008, PMID 15136939
- J. Hadem, H. Wedemeyer, MP Manns: Hepatita ca boală de mișcare. În: Internist. 2004; 45, pp. 655-668, PMID 15118829
- Gert Frösner: Diagnostic modern al hepatitei. ISBN 3-932091-50-7 .
- Stefan Zeuzem: Hepatita C în dialog - 100 de întrebări - 100 de răspunsuri. ISBN 3-13-133391-X .
- German Hepatita C Handbook . Editor: Forumul german privind hepatita C e. V., ISBN 3-00-004025-0 .
- WP Hofmann: Tratamentul pacienților cu hepatită cronică C: standard curent pentru terapia VHC . În: Dtsch Arztebl Int . Nu. 109 (19) , 2012, pp. 352-358 ( recenzie ).
- Gerhard Scheu : Responsabilitatea produsului delict pentru infecțiile cu hepatită C ale pacienților hemofili. Nomos, Baden-Baden 1999, ISBN 3-7890-6385-1 (Autorul a fost președintele comisiei de anchetă a celui de-al 12-lea Bundestag german pe această temă.)
- Hartwig Klinker: infecții cu viruși. În: Marianne Abele-Horn (Ed.): Terapie antimicrobiană. Susținerea deciziilor pentru tratamentul și profilaxia bolilor infecțioase. Cu colaborarea lui Werner Heinz, Hartwig Klinker, Johann Schurz și August Stich, ediția a doua, revizuită și extinsă. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4 , pp. 297-307, aici: pp. 299-301.
Link-uri web
- Hepatita C - informații de la Institutul Robert Koch
- Hepatită de rețea de competență
- Lexicon de laborator: Hepatita C
- Programul Național pentru Hepatita C Departamentul SUA pentru Afaceri al Veteranilor (în limba engleză)
- S3 linia directoare : Diagnosticul și tratamentul infecției cu virusul hepatitei C (VHC) , AWMF numărul de înregistrare 021/012, text integral (PDF) începând cu 2018
- Profilaxia ghidului S3, diagnosticul și tratamentul infecției cu virusul hepatitei C (VHC), nr. Registru AWMF :: 021/012
Dovezi individuale
- ↑ DHC-R-final-2018. Adus pe 4 decembrie 2020 .
- ^ Anunț Premiul Nobel pentru Medicină 2020, Süddeutsche Zeitung , 5 octombrie 2020
- ↑ QL Choo, G. Kuo și colab.: Izolarea unei clone de ADNc derivată dintr-un genom al hepatitei virale non-A, non-B, transmisibil din sânge. În: Știință . Volumul 244, numărul 4902, aprilie 1989, pp. 359-362, PMID 2523562 .
- ↑ Donald B. Smith, Jens Bukh, Carla Kuiken, A. Scott Muerhoff, Charles M. Rice: Clasificare extinsă a virusului hepatitei C în 7 genotipuri și 67 subtipuri: criterii actualizate și resurse web de atribuire a genotipului . În: Hepatologie . bandă 59 , nr. 1 , 2014, ISSN 1527-3350 , p. 318-327 , doi : 10.1002 / hep.26744 , PMID 24115039 , PMC 4063340 (text complet gratuit).
- ↑ Jan Felix Drexler , Victor Max Corman, Marcel Alexander Müller și alții: dovezi pentru Hepacivirusuri noi în rozătoare. În: Agenți patogeni PLoS . 9, nr. 6, 2013 doi: 10.1371 / journal.ppat.1003438
- ↑ S. Fujioka, H. Shimomura și colab.: Prevalența markerilor virusului hepatitei B și C la pacienții ambulatori din spitalele generale mongole. În: Kansensh? Gaku zasshi. Jurnalul Asociației Japoneze pentru Boli Infecțioase. Volumul 72, numărul 1, ianuarie 1998, pp. 5-11, PMID 9503777 .
- ^ Institutul Robert Koch: Buletin epidemiologic . 13/2006.
- ^ Institutul Robert Koch: Buletin epidemiologic. 46/2005.
- ↑ G. Seger: Droguri și hepatită C: dorite noi concepte de prevenire. În: Dtsch Arztebl. Volumul 101, numărul 27, 2004.
- ↑ GL Armstrong, A. Wasley și colab.: Prevalența infecției cu virusul hepatitei C în Statele Unite, 1999 până în 2002. În: Annals of Internal Medicine . Volumul 144, numărul 10, mai 2006, pp. 705-714, PMID 16702586 .
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 18 ianuarie 2002.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 17 ianuarie 2003.
- ↑ Buletinul epidemiologic nr. 2 al RKI (PDF) 16 ianuarie 2004.
- ↑ Buletin epidemiologic nr. 2 al RKI (PDF) 14 ianuarie 2005.
- ↑ Buletin epidemiologic nr. 3 al RKI (PDF) 20 ianuarie 2006.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 19 ianuarie 2007.
- ↑ Buletin epidemiologic nr. 3 al RKI (PDF) 18 ianuarie 2008.
- ↑ Buletin epidemiologic nr. 3 al RKI (PDF) 19 ianuarie 2009.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 25 ianuarie 2010.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 24 ianuarie 2011.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 23 ianuarie 2012.
- ↑ Buletin epidemiologic nr. 3 al RKI (PDF) 21 ianuarie 2013.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 20 ianuarie 2014.
- ↑ Buletinul nr. 3 al RKI (PDF) 14 ianuarie 2015.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 20 ianuarie 2016.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 18 ianuarie 2017.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 17 ianuarie 2018.
- ↑ Buletinul epidemiologic nr. 3 al RKI (PDF) 17 ianuarie 2018.
- ↑ a b Buletin epidemiologic nr. 3 al RKI (PDF) 16 ianuarie 2020
- ↑ Centre pentru controlul și prevenirea bolilor: Întrebări frecvente referitoare la hepatita C pentru profesioniștii din domeniul sănătății
- ↑ Ghid ( Memorie din 12 ianuarie 2012 în Arhiva Internet ) (PDF; 1 MB)
- ↑ Hartwig Klinker: Hepatita C. În: Marianne Abele-Horn (Ed.): Terapie antimicrobiană. Susținerea deciziilor pentru tratamentul și profilaxia bolilor infecțioase. Cu colaborarea lui Werner Heinz, Hartwig Klinker, Johann Schurz și August Stich, ediția a doua, revizuită și extinsă. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4 , pp. 299-301, aici: p. 299 (în studii precum HepNet).
- ↑ a b dgvs.de (PDF)
- ↑ Ira M. Jacobson, Stuart C. Gordon, Kris V. Kowdley, Eric M. Yoshida, Maribel Rodriguez-Torres, Mark S. Sulkowski, Mitchell L. Shiffman, Eric Lawitz, Gregory Everson, Michael Bennett, Eugene Schiff, M. Tarek Al-Assi, G. Mani Subramanian, D. i. An, Ming Lin, John McNally, Diana Brainard, William T. Symonds, John G. McHutchison, Keyur Patel, Jordan Feld, Stephen Pianko, David R. Nelson: Sofosbuvir pentru hepatita C genotipul 2 sau 3 la pacienții fără opțiuni de tratament. În: New England Journal of Medicine. 2013, p. 130423030016000, doi: 10.1056 / NEJMoa1214854 .
- ↑ Eric Lawitz, Alessandra Mangia, David Wyles, Maribel Rodriguez-Torres, Tarek Hassanein, Stuart C. Gordon, Michael Schultz, Mitchell N. Davis, Zeid Kayali, K. Rajender Reddy, Ira M. Jacobson, Kris V. Kowdley, Lisa Nyberg, G. Mani Subramanian, Robert H. Hyland, Sarah Arterburn, Deyuan Jiang, John McNally, Diana Brainard, William T. Symonds, John G. McHutchison, Aasim M. Sheikh, Zobair Younossi, Edward J. Gane: Sofosbuvir pentru Anterior Infecția cronică a hepatitei C netratată. În: New England Journal of Medicine. 2013, p. 130423030016000, doi: 10.1056 / NEJMoa1214853 .
- ↑ C. Neumann-Haefelin, HE Blum, R. Thimme: abordări terapeutice antivirale directe în hepatita cronică C În: Dtsch med Wochenschr. 2012; 137 (25/26), pp. 1360-1365. doi: 10.1055 / s-0032-1305064 .
- ↑ Christoph Sarrazin, Thomas Berg, Peter Buggisch, Matthias Dollinger, Holger Hinrichsen, Dietrich Hüppe, Michael Manns, Stefan Mauss, Jörg Petersen, Karl-Georg Simon, Heiner Wedemeyer, Stefan Zeuzem: Recomandarea actuală a DGVS și a bng pentru terapie hepatitei cronice C ( amintirea originalului din 02 aprilie 2015 în Internet Archive ) Info: arhiva link - ul a fost introdus în mod automat și nu a fost încă verificată. Vă rugăm să verificați linkul original și arhivă conform instrucțiunilor și apoi eliminați această notificare. , Ghidul DGVS; accesat ultima dată pe 8 martie 2015.
- ↑ Comisia Europeană acordă aprobarea lui Harvoni. Adus pe 21 martie 2015 .
- ↑ Tablete TECHNIVIE ™ (ombitasvir, paritaprevir și ritonavir), pentru uz oral. Informații complete de prescriere . AbbVie Inc., North Chicago, IL 60064. Accesat la 28 iulie 2015.
- ↑ Katja Deterding, Norbert Grüner, Peter Buggisch, Johannes Wiegand, Peter R. Galle, Ulrich Spengler, Holger Hinrichsen, Thomas Berg, Andrej Potthoff, Nisar Malek, Anika Großhennig, Armin Koch, Helmut Diepolder, Stefan Lüth, Sandra Feyerabend, Maria Christina Jung, Magdalena Rogalska-Taranta, Verena Schlaphoff, Markus Cornberg, Michael P. Manns, Heiner Wedemeyer: Tratament întârziat versus tratament imediat pentru pacienții cu hepatită C acută: un studiu randomizat controlat de non-inferioritate. În: Boli infecțioase Lancet . 13, 2013, pp. 497-506, doi: 10.1016 / S1473-3099 (13) 70059-8 .
- ↑ FDA aprobă telaprevir, 13 mai 2011 , raport pe Medscape.com, accesat la 26 februarie 2019
- ↑ Istoricul aprobării Victrelis (Boceprevir) pe drug.com, accesat la 26 februarie 2019
- ↑ Hartwig Klinker: Infecții cu virusuri ale hepatitei. În: Marianne Abele-Horn (Ed.): Terapie antimicrobiană. Susținerea deciziilor pentru tratamentul și profilaxia bolilor infecțioase. Cu colaborarea lui Werner Heinz, Hartwig Klinker, Johann Schurz și August Stich, ediția a doua, revizuită și extinsă. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4 , pp. 299-301, aici: pp. 300 f.
- ↑ Informații despre produs de la Agenția Europeană pentru Medicamente pe telaprevir
- ↑ Informații despre produs despre boceprevir de la Agenția Europeană pentru Medicamente
- ↑ Noi medicamente împotriva VHC la AASLD. Natap.org
- ↑ Anna S. Lok și colab.: Studiu preliminar al doi agenți antivirali pentru genotipul hepatitei C 1. În: N Engl J Med , 2012, 366, pp. 216-224.
- ↑ J. Guedja, H. Daharia, L. Rong, ND Sansonee, RE Nettlesh, SJ Cotlere, TJ Laydene, SL Uprichardd, AS Perelson: Modelarea arată că inhibitorul NS5A daclatasvir are două moduri de acțiune și produce o estimare mai scurtă a timpul de înjumătățire plasmatică al virusului hepatitei C. doi: 10.1073 / pnas.1203110110
- ↑ Suntem pregătiți pentru regimuri de tratament fără IFN? Natap.org
- ↑ Rapoarte de conferință pentru NATAP , accesat la 26 martie 2014.
- ↑ Hartwig Klinker (2009), p. 300.
- ↑ Hepatita C: retragere pentru GS-7977 în cazul corespondenților nul cu genotipul 1 . ( Memento de la 1 martie 2012 în Arhiva Internet ) Deutsche Leberhilfe e. V.
- ↑ Ellen Reifferscheid: Introducere nouă în Epclusa. În: Lista Galbenă. Medical Media Informations GmbH, 4 august 2016, accesat la 21 iulie 2017 .
- ↑ Jordan J. Feld, Ira M. Jacobson, Christophe Hézode, Tarik Asselah, Peter J. Ruane, Norbert Gruener, Armand Abergel, Alessandra Mangia, Ching-Lung Lai, Henry LY Chan, Francesco Mazzotta, Christophe Moreno, Eric Yoshida, Stephen D. Shafran, William J. Towner: Sofosbuvir și Velpatasvir pentru VHC Genotip 1, 2, 4, 5 și 6 Infecție . În: New England Journal of Medicine . 16 noiembrie 2015, p. 151117120417004. doi : 10.1056 / NEJMoa1512610 .
- ↑ GT Strickland: Boală hepatică în Egipt: hepatita C a înlocuit schistosomiaza ca urmare a factorilor iatrogeni și biologici. În: Hepatologie . Volumul 43, nr. 5, 2006, pp. 915-922.
- ^ C. Frank și colab.: Rolul terapiei antischistozomiale parenterale în răspândirea virusului hepatitei C în Egipt. În: The Lancet . Volumul 355, nr. 9207, 2000, pp. 887-891.
- ↑ Compensație pentru persoanele infectate cu hepatită C. În: Deutsches Ärzteblatt. Volumul 94, nr. 9, 1997, pp. A-500 / B-422 / C-398. ( aerzteblatt.de )
- ↑ Întrebare majoră a deputaților Horst Schmidbauer și colab. privind infecția cu plasmă contaminată cu hepatită C 1978/1979 în RDG dipbt.bundestag.de Bundestagul german, tipărit 13/1649 din 7 iunie 1995.
- ↑ Bundestag german, (PDF) Tipărit 15/2792 (PDF)
- ↑ Scandalul SIDA: hemofilii cer despăgubiri. În: Hamburger Abendblatt . 17 august 1999, accesat la 1 aprilie 2019 .
- ↑ Elizabeth Kenny-Walsh: Rezultate clinice după infecția cu hepatită C din imunoglobulina anti-D contaminată. În: New England Journal of Medicine. Volumul 340, nr. 16, 1999, pp. 1228-1233.
- ^ S. Barrett și colab.: Cursul natural al infecției cu virusul hepatitei C după 22 de ani într-o cohortă omogenă unică: clearance viral spontan și infecție cronică cu VHC. În: Bine. Volumul 49, 2001, pp. 423-430.
- ↑ Victimele hepatitei C soluționează procesele intentate împotriva statului. În: The Japan Times. 5 februarie 2008. ( search.japantimes.co.jp )
- ↑ Factura de hepatită C care oferă ajutor, scuzele elimină dieta. În: The Japan Times. 12 ianuarie 2008. ( search.japantimes.co.jp )
- ↑ Raportul crește cazurile de expunere la hepatita C la 8.896. În: The Japan Times. 16 februarie 2008. ( search.japantimes.co.jp )
- ↑ Scandal de sânge: Miracole de la Bonn . În: Der Spiegel . Nu. 41 , 1994 ( online ).
- ↑ Cerere pentru o schemă de compensare a hemofilicilor infectați cu VHC prin produse sanguine. Bundestag german, 21 ianuarie 2009; dip21.bundestag.de (PDF)
- ↑ Udo Ludwig: moarte pe bază de prescripție medicală . În: Der Spiegel . Nu. 32 , 2009 ( online ).
- ↑ El ADN revela că el anestesist Maeso Contagio la hepatitis C a 171 pacienți. În: El País. 24 februarie 2000. ( elpais.com )
- ↑ Personalul clinic a folosit seringi contaminate la 40.000 de pacienți - conform instrucțiunilor . În: Spiegel Online , 29 februarie 2008.
- ↑ Prețul Sovaldi a crescut. 16 februarie 2015, accesat pe 13 martie 2021 .
- ↑ Hepatită și altele: Prezentare generală a prețurilor. Adus la 13 martie 2021 .
- ↑ Volker Stollorz: Curește icterul, plătește bine . pe: faz.net , 28 iulie 2014.
- ↑ Rita Flubacher: Un pachet de pastile pentru 19.000 de franci. În: Tages-Anzeiger, 7 august 2014, p. 1.
- ↑ Grupul media Avoxa Deutscher Apotheker GmbH: medicamente inovatoare pentru hepatita C: Care sunt beneficiile suplimentare? Adus la 13 martie 2021 .