Hidrochinona
| Formula structurala | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| General | ||||||||||||||||||||||
| Nume de familie | Hidrochinona | |||||||||||||||||||||
| alte nume |
|
|||||||||||||||||||||
| Formulă moleculară | C 6 H 6 O 2 | |||||||||||||||||||||
| Descriere scurta |
solid incolor și inodor, cristalin |
|||||||||||||||||||||
| Identificatori externi / baze de date | ||||||||||||||||||||||
| ||||||||||||||||||||||
| proprietăți | ||||||||||||||||||||||
| Masă molară | 110,11 g mol -1 | |||||||||||||||||||||
| Starea fizică |
cu fermitate |
|||||||||||||||||||||
| densitate |
|
|||||||||||||||||||||
| Punct de topire |
170 ° C (forma α) |
|||||||||||||||||||||
| Punct de fierbere |
286 ° C |
|||||||||||||||||||||
| Presiunea de vapori |
15 m Pa (20 ° C) |
|||||||||||||||||||||
| pK s valoarea |
|
|||||||||||||||||||||
| solubilitate |
solubil în apă: 72 g l −1 (20 ° C) |
|||||||||||||||||||||
| instructiuni de siguranta | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
|
|||||||||||||||||||||
| În măsura în care este posibil și obișnuit, sunt utilizate unități SI . Dacă nu se specifică altfel, datele furnizate se aplică condițiilor standard . | ||||||||||||||||||||||
Hidrochinona ( 1,4-dihidroxibenzen ) este un fenol și, alături de pirocatechol (1,2-dihidroxibenzen) și resorcinol (1,3-dihidroxibenzen), este al treilea dihidroxibenzen posibil. Aici cele două grupări hidroxil sunt în poziția para .
descoperire
În 1844 Friedrich Wöhler a obținut un amestec de produse din distilarea uscată (> 280 ° C) a acidului chinic care, pe lângă benzen , acid benzoic și acid salicilic, conținea un nou compus incolor ca component principal. După dizolvarea distilatului în apă, filtrarea componentelor insolubile și distilarea componentelor mai volatile, acidul benzoic a cristalizat mai întâi din soluția rămasă și în cele din urmă hidrochinonă din lichiorul său mamă, pe care l-a obținut în formă pură prin recristalizare repetată sub formă de incolor , prisme cu șase fețe.
Apariție
Hidrochinona apare ca o soluție de aproximativ 10% împreună cu 28% peroxid de hidrogen în glandele de apărare ale gândacilor bombardieri . În caz de apărare, se adaugă catalază amestecului și atacatorul este pulverizat sub formă de repelent fierbinte, coroziv de 100 ° C. Ursului frunze precum și pere conțin glycoside Arbutin , care este hidrochinona-β-D-glucozid, un compus hidrochinonei cu glucoză .
prezentare
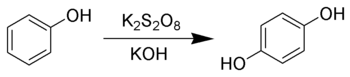
Hidrochinona poate fi sintetizată din fenol prin oxidarea Elbs .
proprietăți
Hidrochinona este un solid incolor care poate apărea în patru forme de cristale polimorfe . Formele α, β și γ există sub presiune normală . Formele α și β cristalizează într-o rețea de cristal hexagonală , γ se formează într-o rețea monoclinică . La temperatura camerei, forma α este forma termodinamic stabilă. Formele β și γ sunt metastabile și se pot transforma spontan în forma α. Forma α corespunde produsului comercial. Forma β poate fi obținută din clatrați cu molecule mici, cum ar fi metanolul . Forma γ poate fi obținută prin sublimare sau evaporare rapidă. La presiuni mai mari de peste 40 MPa, forma can poate fi detectată ca a patra formă cristalină. Punctul de topire al formei δ este de 78,5 MPa la 191 ° C. Punctul triplu dintre a, δ și faza lichidă este de 176 ° C și 15,7 MPa.
Hidrochinona este un agent de reducere mai puternic decât catecolul, deoarece o-benzoquinona produsă din catecol este mai energică și, prin urmare, un oxidant mai puternic. Cauza acestuia din urmă este repulsia electrostatică a grupărilor carbonil vecine.
Poate fi transformat în benzoquinonă ( chinonă ) prin oxidare :
În această reacție, complexul chinhidronă de transfer de sarcină de culoare profundă, slab solubil în apă ( neprezentat ) este format ca produs intermediar .
Reacții
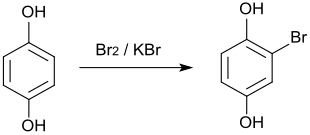
Bromurarea simplă a hidroquinonei cu bromură de potasiu și brom în tetraclorură de carbon duce la bromohidrochinonă .
Bromurarea completă pentru detectarea analitică este asigurată de 2,5-dibromohidrochinonă , al cărei punct de topire este de 186 ° C. De asemenea, este cunoscută tetrabromohidrochinona , care este totuși prezentată pentru benzoquinonă.
Metilarea cu sulfat de dimetil dă 1,4-dimetoxibenzen , al cărui punct de topire este de 56 ° C.
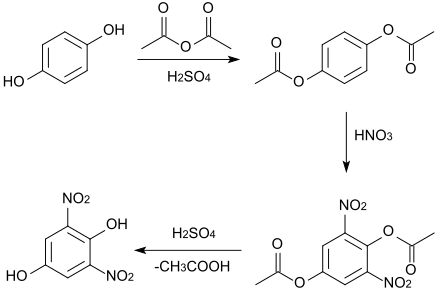
Nu este posibilă nitrarea directă a hidrochinonei, deoarece se descompune în proces. Prin urmare, grupările hidroxil trebuie protejate cu grupări acetil prin reacție cu anhidridă acetică și acid sulfuric ca catalizator , apoi nitrarea are loc în pozițiile 2 și 6. Saponificarea dinitrodiacetilhidrochinonei rezultate duce în cele din urmă la 2,6-dinitrohidrochinonă (punct de topire 135-136 ° C).
utilizare
În tehnologia de laborator foto, hidrochinona este utilizată ca agent de reducere pentru dezvoltarea filmelor și imaginilor. Din cauza pericolelor pentru mediu și sănătate, se fac eforturi pentru a înlocui substanța pentru aceste aplicații cu substanțe mai puțin riscante, dacă este posibil. De asemenea, este utilizat ca inhibitor al reacțiilor radicale pentru a preveni formarea de peroxizi eterici.
Utilizarea cosmetică în cremele de piele, de exemplu pentru iluminarea pielii , este interzisă în țările UE.
toxicologie
Nu există studii privind toxicitatea directă a hidrochinonei la om. Cu toate acestea, mai multe studii pe animale au arătat că hidroquinona este toxică pentru rinichi. În plus, hidrochinona este imunotoxică și probabil joacă, de asemenea, un rol important în imunotoxicitatea benzenului .
Dacă hidroquinona este aplicată dermic, pot apărea reacții alergice și alergice sistematice.
Cancerogenitate
Două studii de cohortă sunt disponibile pe oameni, unul de litografi danezi și unul de muncitori industriali, în care a fost investigată relația dintre expunerea la hidrochinonă și apariția cancerului în general, precum și a tumorilor specifice. O conexiune nu a putut fi stabilită în niciunul dintre cele două studii, chiar dacă incidența melanomului a fost crescută în rândul litografilor .
În experimentele la șobolani, administrarea repetată de hidrochinonă a arătat o incidență crescută a anumitor tumori la nivelul ficatului și rinichilor.
Prin urmare, se presupune că hidroquinona, ca și alte dihidroxibenzeni (de exemplu, catecol), este cancerigenă și genotoxică.
Posibile mecanisme de acțiune
În experimentele pe celule hepatice , hidrochinona a condus la o epuizare a antioxidanților din celulă, în special glutation . În plus, s-ar putea arăta în cultura celulară că hidrochinona formează aducti ADN și crește formarea de 8-OHdG , un marker standard pentru deteriorarea ADN-ului. Se crede că această deteriorare a ADN-ului este legată de formarea ROS.
metabolism
La om, hidrochinona este metabolizată în principal pentru a forma conjugați sulfat și glucoronidă. În plus față de intermediarii reactivi, cum ar fi semiquinonele și ROS , 1,4-benzoquinona se formează, de asemenea, în cadrul acestor căi metabolice . Acest metabolism este catalizat de o serie de oxidaze . Metabolismul hidroquinonei este astfel similar cu cel al catecolului .
Evaluarea pericolelor
Hidrochinona a fost inclusă de UE în 2012 în conformitate cu Regulamentul (CE) nr. 1907/2006 (REACH) ca parte a evaluării substanței în planul de acțiune în curs al Comunității ( CoRAP ). Efectele substanței asupra sănătății umane și a mediului sunt reevaluate și, dacă este necesar, sunt inițiate măsuri de urmărire. Ingerarea de hidrochinonă a fost determinată de îngrijorarea cu privire la clasificarea sa ca substanță CMR , utilizarea consumatorilor , tonajul ridicat (agregat), raportul de caracterizare a riscului ridicat (RCR) și utilizarea pe scară largă. Reevaluarea a avut loc din 2012 și a fost efectuată de Italia . Apoi a fost publicat un raport final.
Dovezi individuale
- ↑ Intrare pe HIDROQUINONĂ în baza de date CosIng a Comisiei UE, accesată la 14 mai 2020.
- ↑ a b c d e f g h i Intrare pentru CAS nr. 123-31-9 în baza de date a substanței GESTIS IFA , accesat la 06 decembrie 2015. (JavaScript este necesar)
- ^ A b S. C. Wallwork, HM Powell: Structura cristalină a formei α a chinolului. În: J. Chem. Soc. Perkin Trans. Vol. 2, 1980, pp. 641-646, doi: 10.1039 / P29800000641 .
- ↑ a b c S. V. Lindemann, VE Shklover, Yu. T. Struchkov: β-modificarea hidroquinonei, C6H6O2. În: Cryst. Struct. Comun. Volumul 10, 1981, pp. 1173-1179.
- ↑ a b c K. Maartmann-Moe: Structura cristalină a γ-hidroquinonei. În: Acta Cryst. Volumul 21, 1966, pp. 979-982, doi: 10.1107 / S0365110X66004286 .
- ↑ a b intrare pe hidrochinonă. În: Römpp Online . Georg Thieme Verlag, accesat la 2 august 2018.
- ↑ Intrare pe hidrochinonă în inventarul de clasificare și etichetare al Agenției Europene pentru Produse Chimice (ECHA), accesat la 1 februarie 2016. Producătorii sau distribuitorii pot extinde clasificarea și etichetarea armonizate .
- ↑ Fondul elvețian de asigurare a accidentelor (Suva): valori limită - valorile actuale MAK și BAT (căutare 123-31-9 sau hidrochinonă ), accesat la 2 noiembrie 2015.
- ↑ F. Wöhler: Despre chinonă. În: Pharmaceutisches Centralblatt . 39, 1844, pp. 609-615. ( previzualizare limitată în căutarea Google Book).
- ↑ H. Schildknecht, K. Holoubekal: Gândacii bombardieri și chimia exploziei lor. În: Angewandte Chemie . 73 (1), 1961, pp. 1-7. doi: 10.1002 / anie.19610730102 .
- ↑ Werner Nachtigall, A. Wisser: Proiectare biologică. Prima ediție. Springer-Verlag, Berlin 2005, ISBN 3-540-22789-X . ( previzualizare limitată în căutarea Google Book).
- ↑ Gerhard G. Habermehl: Animalele otrăvitoare și armele lor. 5, actualizat și exp. Ediție. Springer-Verlag, Berlin 1994, ISBN 3-540-56897-2 . ( previzualizare limitată în căutarea Google Book).
- ↑ K. Elbs: Despre Nitrohidrochinonă. În: J. Prakt. Chem. 48, 1893, pp. 179-185. doi: 10.1002 / prac.18930480123 .
- ↑ WA Caspari: Structura cristalină a chinolului. Partea I. În: J. Chem. Soc. 1926, p. 2944-2248. doi: 10.1039 / JR9262902944 .
- ↑ a b c W. A. Caspari: Structura cristalină a chinolului. Partea II În: J. Chem. Soc. 1927, p. 1093-1095. doi: 10.1039 / JR9270001093 .
- ↑ a b c d e M. Naoki, T. Yoshizawa, N. Fukushima, M. Ogiso, M. Yoshino: O nouă fază a hidrochinonei și a proprietăților sale termodinamice. În: J. Phys. Chem. B 103, 1999, pp. 6309-6313. doi: 10.1021 / jp990480k .
- ^ DE Palin, HM Powell: Legătura cu legătura de hidrogen a moleculelor de chinol. În: Natura . Volumul 156, 1948, p. 334. doi: 10.1038 / 156334a0 .
- ^ DE Palin, HM Powell: Structura compușilor moleculari. Partea a III-a. Structura cristalină a complexelor de adiție a chinolului cu anumiți compuși volatili. În: J. Chem. Soc. 1947, pp. 208-221. doi: 10.1039 / JR9470000208 .
- ^ DE Palin, HM Powell: Structura compușilor moleculari. Partea a VI-a. Compușii clatrat de tip β ai chinolului. În: J. Chem. Soc. 1948, pp. 815-821. doi: 10.1039 / JR9480000815 .
- ^ Asociația autorilor: Organikum . Ediția a 19-a. Johann Ambrosius Barth, Leipzig / Berlin / Heidelberg 1993, ISBN 3-335-00343-8 , p. 331.
- ↑ M. Kohn, LW Guttmann: Despre cunoașterea produselor de substituție a bromului de hidrochinonă. În: Revista lunară pentru chimie . 45 (10), 1924, pp. 573-588. doi: 10.1007 / BF01524599 .
- ^ Asociația autorilor: Organikum . Ediția a 19-a. Johann Ambrosius Barth, Leipzig / Berlin / Heidelberg 1993, ISBN 3-335-00343-8 , p. 653.
- ↑ a b Gustav Walther: eter metilic al 2,6-dinitrohidroquinonei și alți derivați. Disertație. Universitatea din Basel, 1904.
- ↑ H. Bock, S. Nick, C. Näther, JW Bats: Nitranilat disodic și dipotasic: distorsiunea cianină a inelelor cu șase membri ai carbonului. In: Journal of Nature Research B . 49, 1994, pp. 1021-1030 ( PDF , text complet gratuit).
- ↑ https://ec.europa.eu/growth/tools-databases/cosing/index.cfm?fuseaction=search.results&annex_v2=II&search
- ↑ Programul Național de Toxicologie: Studii de Toxicologie și Carcinogeneză NTP ale Hidrochinonei (CAS Nr. 123-31-9 ) la Șobolani F344 / N și Șoareci B6C3F1 (Studii Gavage) . În: Programul național de toxicologie Seria de rapoarte tehnice . bandă 366 , octombrie 1989, ISSN 0888-8051 , p. 1-248 , PMID 12692638 .
- ↑ Masa-Aki Shibata, Masao Hirose, Hikaru Tanaka, Emiko Asakawa, Tomoyuki Shirai: inducerea tumorilor de celule renale la șobolani și șoareci și îmbunătățirea dezvoltării tumorilor hepatocelulare la șoareci după tratamentul pe termen lung cu hidrochinonă . În: Jurnalul japonez de cercetare a cancerului . bandă 82 , nr. 11 , 1991, ISSN 1349-7006 , pp. 1211-1219 , doi : 10.1111 / j.1349-7006.1991.tb01783.x , PMID 1752780 , PMC 5918322 (text complet gratuit).
- ↑ a b Agenția Internațională pentru Cercetarea Cancerului: Reevaluarea unor substanțe chimice organice, hidrazină și peroxid de hidrogen. Organizația Mondială a Sănătății, Agenția Internațională pentru Cercetarea Cancerului, Lyon, Franța 1999, ISBN 978-92-832-1271-3 .
- ↑ A. Barbaud, P. Modiano, M. Cocciale, S. Reichert, J.-L. Murdărie: Aplicarea topică a resorcinolului poate provoca o reacție alergică sistemică . În: British Journal of Dermatology . bandă 135 , nr. 6 , 1996, ISSN 1365-2133 , pp. 1014-1015 , doi : 10.1046 / j.1365-2133.1996.d01-1121.x .
- ↑ JW Pifer, FT Hearne, FA Swanson, JL O'Donoghue: Studiul mortalității angajaților angajați în fabricarea și utilizarea hidrochinonei . În: Arhivele internaționale de sănătate a muncii și a mediului . bandă 67 , nr. 4 , 1995, ISSN 0340-0131 , p. 267-280 , doi : 10.1007 / BF00409409 , PMID 7591188 .
- ^ Vol Carlton, H Shah: Re: "Melanomul malign printre litografi" de H Nielsen, L Henriksen, JH Olsen. Scand J Work Environ Health 1996; 22: 108-11 . În: Scandinavian Journal of Work, Environment & Health . bandă 23 , nr. 4 , august 1997, ISSN 0355-3140 , p. 308 , doi : 10.5271 / sjweh.224 .
- ↑ a b U. Stenius, M. Warholm, A. Rannug, S. Walles, I. Lundberg: Rolul epuizării și toxicității GSH în dezvoltarea indusă de hidroquinonă a focarelor modificate enzimatic . În: Carcinogeneză . bandă 10 , nr. 3 , martie 1989, ISSN 0143-3334 , p. 593-599 , doi : 10.1093 / carcin / 10.3.593 , PMID 2564322 .
- ↑ Junzo Suzuki, Yuichiro Inoue, Shizuo Suzuki: Modificări ale nivelului de excreție urinară a 8-hidroxiguaninei prin expunerea la substanțe reactive generatoare de oxigen . În: Biologie și medicină radicală liberă . bandă 18 , nr. 3 , 1 martie 1995, ISSN 0891-5849 , p. 431-436 , doi : 10.1016 / 0891-5849 (94) 00152-A ( sciencedirect.com [accesat la 30 iunie 2020]).
- ↑ G. Lévay, WJ Bodell: Rolul peroxidului de hidrogen în formarea aductelor ADN în celulele HL-60 tratate cu metaboliți benzenici . În: Comunicări de cercetare biochimică și biofizică . bandă 222 , nr. 1 , 6 mai 1996, ISSN 0006-291X , p. 44-49 , doi : 10.1006 / bbrc.1996.0695 , PMID 8630072 .
- ^ G. Levay, K. Pongracz, WJ Bodell: Detectarea aductelor ADN în celulele HL-60 tratate cu hidrochinonă și p-benzoquinonă prin postetichetare 32P . În: Carcinogeneză . bandă 12 , nr. 7 , iulie 1991, ISSN 0143-3334 , pp. 1181-1186 , doi : 10.1093 / carcin / 7.12.1181 , PMID 2070482 .
- ↑ Organizația Mondială a Sănătății: Hidrochinonă . În: Organizația Mondială a Sănătății (Ed.): Criterii de sănătate a mediului . bandă 157 . Geneva 1994.
- ^ BA Hill, HE Kleiner, EA Ryan, DM Dulik, TJ Monks: Identificarea conjugatului multi-S-substituit al hidroquinonei prin analiza matricei de electrod coulometric HPLC și spectroscopie de masă . În: Cercetări chimice în toxicologie . bandă 6 , nr. 4 , iulie 1993, ISSN 0893-228X , p. 459-469 , doi : 10.1021 / tx00034a012 , PMID 8374043 .
- ↑ Vangala V. Subrahmanyam, Prema Kolachana, Martyn T. Smith: Metabolismul hidrochinonei prin mieloperoxidaza umană: Mecanisme de stimulare de către alți compuși fenolici . În: Arhive de biochimie și biofizică . bandă 286 , nr. 1 , 1 aprilie 1991, ISSN 0003-9861 , pp. 76-84 , doi : 10.1016 / 0003-9861 (91) 90010-G ( sciencedirect.com [accesat la 30 iunie 2020]).
- ↑ Agenția Europeană pentru Produse Chimice (ECHA): concluzia evaluării substanțelor și raportul de evaluare .
- ↑ Planul comunitar de acțiune continuă ( CoRAP ) al Agenției Europene pentru Produse Chimice (ECHA): Hidrochinonă , accesat la 26 martie 2019.