Chist rinichi
| Clasificare conform ICD-10 | |
|---|---|
| Q61.1 | Rinichi polichistic, tip autosomal recesiv infantil |
| Q61.2 | Rinichi polichistic, tip adult autosomal dominant |
| Q61.3 | Rinichiul polichistic, nespecificat |
| ICD-10 online (versiunea OMS 2019) | |

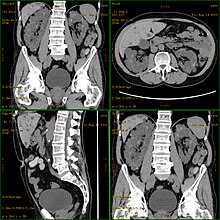
Boli de rinichi polichistic , de asemenea , cunoscut sub numele de rinichi polichistic desemnat ( engleza rinichi polichistic boala , CPD sunt un grup de grave, mai ales) ereditare înrudite cu boli ale rinichilor . Datorită formării unui număr mare ( antice grecești πολύς poligoane „mult“) de camere sau vezicule umplute cu lichid, așa-numitele chisturi , rinichii sunt considerabil mai limitate în lor funcție de filtrare . Un chist renal , pe de altă parte, este un singur chist care este de obicei menționat ca o descoperire inofensivă a șanselor în cursul unei examinări .
Chisturile renale determinate genetic sunt cele mai frecvente boli ereditare care pun viața în pericol la om și una dintre principalele cauze ale insuficienței renale cronice . O vindecare este posibilă numai cu un transplant de rinichi .
Simptome
Primele simptome care pot indica rinichii chistici sunt hipertensiunea arterială , urină sângeroasă ( hematurie ), infecții repetate ale tractului urinar , o creștere a dimensiunii abdomenului și durere în abdomen. Atâta timp cât rinichii pot compensa orice afectare funcțională, adesea nu există simptome. Aproximativ o treime din pacienți rămân fără simptome , chiar până la insuficiența renală în stadiul final (ESRF). Acest lucru face un diagnostic precoce mult mai dificil. Distrugerea crescândă a țesutului renal duce la tot mai multe plângeri în diferite organe din cauza deșeurilor reținute și a apei. Acestea includ scăderea performanței și stare de rău, îngălbenirea și mâncărimea pielii din cauza toxinelor urinare stocate, tulburări de somn și concentrare, dureri de cap, crampe de vițel, greață, vărsături, diaree și tulburări de gust. Apar de asemenea tensiune arterială crescută, aritmii sau inflamații cardiace și probleme de respirație. În plus, există anemie (datorită reducerii eritropoietinei produse de rinichi, care este utilizată pentru formarea sângelui), tulburări de coagulare, susceptibilitate crescută la infecții, sângerări cerebrale și înmuierea oaselor (deoarece rinichiul este implicat și în metabolismul vitaminei D).
Pacienții cu rinichi polichistic se plâng adesea de dureri în flancul lateral al spatelui sau al abdomenului . Durerea poate fi temporară sau permanentă, plictisitoare și chinuitoare. Durerea se datorează probabil creșterii extinse a chistului. În plus, organele din jur sunt deplasate de întinderea extremă a capsulei renale (Capsula fibrosa renalis) .
Durerea poate fi ameliorată pentru scurt timp prin puncția chisturilor, de exemplu , percutanat , adică prin piele, sau minim invaziv prin decorticarea laparoscopică a chisturilor. Datorită formării de chisturi noi, aceste măsuri nu sunt durabile, astfel încât intervențiile corespunzătoare trebuie repetate. În plus, tratamentul nu modifică cursul bolii.
La aproximativ 30-50% dintre pacienți, diagnosticul inițial de „rinichi polichistic” se face din urină sângeroasă ( hematurie ). Cauza sângerării este de obicei fisurile din chisturi. Sângerarea în sine este în mare parte inofensivă și se oprește de la sine. Datorită funcției renală, pacienții cu rinichi chistice excreta cantitati de endogene a crescut de proteine in urina . Dacă corpul excretă 30 până la 300 miligrame de albumină pe zi , se numește microalbuminurie . Dacă se excretă și cantități mai mari de albumină, aceasta se numește macroalbuminurie . Dacă proteinele mai mari decât albumina pot fi detectate în urină, proteinuria este prezentă. Acesta din urmă poate fi ușor detectat cu benzi de testare care sunt ținute în urină. Microalbuminuria este mult mai dificil de detectat. Proteinele și microalbuminuria sunt o indicație a afectării funcției renale. Rinichii polichistici sunt doar una dintre mai multe afecțiuni posibile care pot duce la această disfuncție.
O hipertensiune arterială („hipertensiune arterială”) este localizată în fața pacienților cu rinichi polichistic la 50 până la 75%. Tensiunea arterială a celor afectați este adesea deja crescută semnificativ înainte de scăderea funcției renale ( rata de filtrare glomerulară , GFR).
Diagnostic

Diagnosticul se face de obicei prin sonografie („ultrasunete”) sau prin alte metode imagistice , cum ar fi tomografia prin rezonanță magnetică . Cu ultrasunete, chisturile până la o dimensiune de 5 mm pot fi diagnosticate cu dispozitive moderne. Rata de detectare precoce la pacienții în vârstă de 20 de ani este de aproximativ 90%. Deși tomografia computerizată oferă o rezoluție mai mare cu o calitate a imaginii mai bună, nu este utilizată pentru screening-ul pacientului , în primul rând din cauza expunerii la radiații , ci doar pentru întrebări de diagnostic speciale.
Biopsie , în care se îndepărtează o cantitate mică de țesut de rinichi și ficat, este utilizat în copilărie pentru a diferenția între ARPKD și ADPKD ( debut precoce ) . Aceasta înseamnă că modificările morfologice ale membranei bazale pot fi detectate într-un stadiu foarte timpuriu. ARPKD este diagnosticat prin determinarea fibrozei congenitale a ficatului .
Potrivit lui Osathanondh și Potter , rinichii chistului sunt divizați patologic și anatomic în următoarele tipuri:
| Tip | Infestare | Dimensiunea rinichilor | Dimensiunea chistului | Glomeruli | Chisturi ale căilor biliare | Timpul de supraviețuire |
|---|---|---|---|---|---|---|
| I. | ambele părți | mărit la mult mărit | lățime uniformă (12 mm) | normal | disponibil | Perioada neonatală |
| II | față-verso, față-verso sau parțial | mărită sau redusă | de dimensiuni diferite | diminuat și anormal | indisponibil | Maturitate |
| III | mai ales bilaterale | mărită | diferite dimensiuni, uneori foarte departe | chisturi glomerulare | ocazional, dar apoi numai în zone circumscrise | Maturitate |
| IV | ambele părți | micșorat | mici, situate subcapsular | Glomerulii diminuează, chisturile glomulare | indisponibil | Maturitate |
Cu toate acestea, în practică, tipurile astfel definite nu permit adesea o clasificare clară . În plus față de descrierea patoanatomică a rinichilor și a ficatului, istoricul familial ( anamneză ) joacă, prin urmare, un rol important. Pentru cazurile ereditare de chisturi renale, termenii genetici autozomali - dominanți și autozomali recesivi sunt de obicei folosiți.
Prin identificarea genelor potențial afectate, este posibil un diagnostic genetic non-invaziv demonstrativ molecular . În multe cazuri, această procedură poate înlocui diagnosticul de biopsie invazivă și permite clasificarea etiologică . La rândul său, această clasificare deschide căi pentru opțiuni terapeutice diferențiale pentru tratarea bolii. Sensibilitatea pentru un rezultat pozitiv într - adevăr este în jur de 95%. O corelație între genotip și fenotip este posibilă doar într-o măsură limitată. Analiza mutației este dificilă cu gena PKD1 datorită dimensiunii sale (46 exoni codificatori și 14,2 kb ai transcrierii ). În plus, primii 33 de exoni ai PKD1 în trei copii omoloage ale cromozomului 16 afectat pe locusul genei p13.1 (HG-A ≈21 kb, HG-B ≈17 kb și HG-C ≈8.5 kb; HG = genă omologă ) sunt prezenți. Acest lucru face ca multiplicarea specifică prin intermediul reacției în lanț a polimerazei (PCR) să fie mult mai dificilă .
Din diagnosticul genetic molecular apare o anumită problemă. Diagnosticul precoce al predispoziției genetice a pacientului permite măsuri profilactice și terapie de susținere timpurie, pe de o parte . Pe de altă parte, rudele și pacienții se pot confrunta cu probabilitatea apariției unei boli care pune viața în pericol în câteva decenii încă din copilărie. Prin urmare, riscurile și beneficiile trebuie cântărite cu atenție înainte de diagnostic.
La pacienții cu dispoziție familială ( predispoziție ), diagnosticul poate fi pus prin sonografie de la vârsta de 20 de ani dacă pot fi detectate cel puțin două chisturi renale pe rinichi. Chisturile lipsă, pe de altă parte, exclud boala la cei cu vârsta peste 30 de ani.
Patogenie
Originea și dezvoltarea rinichilor chistici, patogeneza , se bazează pe o degenerare chistică a așa-numiților tubuli (tubuli renali, de asemenea: tubuli urinari) în rinichi. În cazul PKD moștenit autosomal dominant, acest lucru duce la creșterea crescută a rinichilor în decursul deceniilor. Acest lucru poate duce la afectarea funcțională sau chiar pierderea completă a funcției de filtrare a rinichilor. Ambii rinichi sunt la fel de afectați. Câteva sute de chisturi, care sunt voluminoase ca aspect, se pot dezvolta pe organ. Ca urmare, masa și volumul rinichilor pot crește semnificativ. În timp ce un rinichi sănătos are o masă medie de 160 g , rinichii polichistici pot ajunge până la 8 kg cu un volum de până la 40 × 25 × 20 cm³ (= 20 litri) (rinichi sănătos: 12 × 6 × 3 cm³ = 0,216 litri ). În ciuda creșterii semnificative a spațiului organului, tulburările funcționale ale organelor vecine apar relativ rar.
Chisturile se găsesc atât pe medulla renală (medulla renis), cât și pe cortexul renal (cortex renalis) . În principiu, orice zonă a unui nefron poate dezvolta un chist. Cu toate acestea, glomerulii și ansa Henle sunt afectate în primul rând . Chisturile sunt umplute cu ceea ce este cunoscut sub numele de urină tubulară . Diametrul unui singur chist poate varia foarte mult de la câțiva milimetri la peste 100 mm. Chisturile mari pot conține câteva sute de mililitri de urină tubulară. Interiorul chistului constă dintr - un singur strat epiteliu scuamos sau cu un singur strat isoprismatic (cubic) epiteliu . Pe măsură ce boala progresează, atât numărul cât și dimensiunea chisturilor prezente pot crește.
etiologie
Modificările polichistice ale rinichilor sunt o afecțiune care apare în mai multe boli. Acestea pot apărea sporadic ca o abatere de la dezvoltarea normală a rinichilor sau pot fi dobândite în viața adultă ( rinichi chistici dobândiți) . Cauza mult mai frecventă ( etiologia ) pentru această boală sunt defectele moștenite ale anumitor gene ( rinichii chistici ereditari ) . De departe cea mai mare parte este luată de boala de rinichi autosomal dominanta polichistic ( engleza boala autozomal dominanta de rinichi polichistic , ADPKD ). Această boală este cea mai frecventă cauză ereditară a insuficienței renale cronice : aproximativ 7% din toți pacienții cu dializă suferă de aceasta.
În plus, diverse alte boli ereditare - mult mai rare - provoacă rinichi chistici. Rinichii chistici dobândiți se pot dezvolta și în special la pacienții cu dializă. Deoarece marea majoritate a rinichilor chistici sunt cauzate de ADPKD, termenul „rinichi chistic” este adesea folosit sinonim pentru ADPKD.
Rinichi chistici ereditari
Majoritatea bolilor renale polichistice sunt ereditare ( ereditare ). Un număr mare de gene diferite pot fi afectate și astfel pot declanșa boala. Sindroamele enumerate mai jos reprezintă o selecție a celor mai importante boli renale polichistice ereditare. Unele dintre boli sunt incluse în așa-numitul complex NPH-MCKD .
| genă | Locusul genei cromozomiale |
proteină | maladie | Incidenţă | Vârsta ∗) |
|---|---|---|---|---|---|
| Autosomal dominant | |||||
| PKD1 | 16 p13.3 | Polichistina-1 | ADPKD | 1: 500-1000 | aproximativ 50 |
| PKD2 | 4 q21-q23 | Polichistina-2 | ADPKD | 1: 3500-7000 | aproximativ 70 |
| VHL | 3 p26-p25 | VHL30 | Von-Hippel-Lindau | 1: 35.000 | 20-30 |
| TSC1 | 9 q34 | Hamartin | Scleroză tuberoasă | 1: 10.000 (ambele împreună) | 30-40 |
| TSC2 | 16 p13.3 | Tuberină | Scleroză tuberoasă | ||
| ? | 1 q21 | Boli renale chistice medulare de tip 1 | 1 la 9: 1.000.000 (tip 1 + 2) | 62 | |
| UMOD | 16 p12.3 | Uromodulină | Boala renală chistică medulară de tip 2 | 32 | |
| Autosomal recesiv | |||||
| PKHD1 | 6 p21.2-p12 | Fibrocistina | ARPKD | 1: 20.000 | <20 |
| NPHP1 | 2 q13 | Nefrocistină-1 | Nephronophthisis (juvenil) | aproximativ 1: 100.000 (toate NPHP) | 13 |
| NPHP2 | 9 q22-q31 | Invers | Nefronoftiză (infantilă) | <1 | |
| NPHP3 | 3 q22.1 | Nefrocistină-3 | Nefronoftiză (adolescent) | 19 | |
| NPHP4 | 1 p36,22 | Nefroretinină | Nephronophthisis | 21 | |
| NPHP5 | Nefrocistină 5 | Nephronophthisis | 13 | ||
| NPHP6 | Nefrocistină 6 | Nephronophthisis | |||
| GLIS2 | 16 p13.3 | GLI-Similar Protein 2 | Nephronophthisis | ||
| BBS1 | 11 q13.1 | Proteina BBS1 | Sindromul Bardet-Biedl | 1: 140.000 (toate BBS) | |
| BBS2 | 16 q21 | Proteina BBS2 | Sindromul Bardet-Biedl | ||
| ARL6 | 3 p13-p12 |
Proteina BBS3 ADP-proteină asemănătoare factorului de ribozilare 6 |
Sindromul Bardet-Biedl | ||
| BBS4 | 15 q22.3-q23 | Proteina BBS4 | Sindromul Bardet-Biedl | ||
| BBS5 | 2 q31.1 | Proteina BBS5 | Sindromul Bardet-Biedl | ||
| MKKS | 20 p12 | Proteina BBS6 | Sindromul McKusick-Kaufman | ||
| BBS7 | 4 q27 | Proteina BBS7 | Sindromul Bardet-Biedl | ||
| TTC8 | 14 q31.3 | Proteina BBS8 | Domeniul de repetare tetratricopeptidă 8 | ||
| BBS9 | 7 p14 | PTHB1 | Sindromul Bardet-Biedl | ||
| BBS10 | 12 q21.2 | Proteina BBS10 | Sindromul Bardet-Biedl | ||
| TRIM32 | 9 q33.1 | Proteina de deget de zinc HT2A | 32 de motive tripartite | ||
| BBS12 | 4 q27 | Proteina BBS12 | Sindromul Bardet-Biedl | ||
| Dominant legat de X. | |||||
| CXORF5 | X p22.3-p22.2 | OFD1 | Sindromul oro-facio-digital tip 1 | 1: 250.000 | |
| Moștenire necunoscută | |||||
| ? | ? | Rinichi de chist medular | 1: 5000 | 40-50 | |
| ? | ? | Displazia renală multicistică | <10 și 50-60 |
Boală renală polichistică autosomală dominantă
Boala renală polichistică autosomală dominantă (ADPKD), cunoscută și sub denumirea de degenerescență renală chistică de tip III , este cea mai frecventă boală ereditară care pune viața în pericol la om. Există aproximativ 5 milioane de persoane afectate de ADPKD în întreaga lume. Incidența este de 1: 500-1: 1000. De exemplu, în Statele Unite, este de două ori mai frecventă decât scleroza multiplă și de zece ori mai frecventă decât anemia falciformă . Bărbații și femeile sunt la fel de afectați. Rasa și originea sunt, de asemenea, irelevante. De Simptomele sunt , de obicei observate doar la varsta adulta. Moștenirea ADPKD este autosomală dominantă ( monogenă ) cu penetranță completă . Datorită moștenirii autozomale dominante, jumătate dintre copii moștenesc gena mutantă de la părinți pe o medie statistică și vor dezvolta ei înșiși ADPKD. Aproximativ 50% din toți purtătorii de mutație suferă de insuficiență renală progresivă. La o vârstă medie de 58 de ani, terapia de substituție renală este indicată la jumătate dintre pacienții cu ADPKD .
Ca boală sistemică în ADPKD, alte organe - în majoritatea cazurilor ficatul - sunt adesea afectate de formarea chistului. În funcție de autor, până la 75% dintre cei afectați de ADPKD au chisturi hepatice.
genetică
Până în prezent, mutațiile în două gene diferite au fost identificate ca fiind cauza bolii la pacienții cu ADPKD: genele PKD1 și PKD2 . La om, PKD1 este localizat pe locusul genetic al cromozomului 16 16p13.3-p13.12. Acesta codifică pentru proteina polycystin-1 . La pacienții cu mutații semnificative în PKD1, insuficiența renală atinge stadiul final la o vârstă medie de 50 de ani, ceea ce înseamnă că este indicată terapia de substituție renală. Pacienții cu mutații în PKD2, care se află pe locusul genei cromozomului 4 q21-q23 și codifică policistina-2, ajung în acest stadiu considerabil mai târziu, la o vârstă medie de 70 de ani ( debut tardiv ) . Aproximativ 85% dintre pacienții cu ADPKD poartă una sau mai multe mutații în PKD1. Restul de 15% se datorează mutațiilor din PKD2.
La nivel celular, ADPKD este un mecanism recesiv. Prima condiție pentru boală este o mutație a liniei germinale într-una dintre alelele PKD1 sau PKD2 . În al doilea rând, trebuie să aibă loc o mutație somatică , așa-numita a doua lovitură, astfel încât să se inițieze formarea chistului. Această pierdere de heterozigozitate ( pierderea heterocigozității , LOH) constatată în ADPKD durează în mod evident pentru totdeauna. Mutația somatică inițială poate fi pe cealaltă genă. În acest caz, numită transheterozigoză , mutația liniei germinale este PKD1, iar mutația somatică este PKD2 sau invers. La modelele animale, s-a constatat că mutațiile liniei germinale care afectează ambele alele ale unei gene PKD sunt perinatale fatale. Odată cu a doua lovitură , celula afectată își pierde capacitatea de a inhiba proliferarea și astfel devine punctul de plecare pentru formarea unui nou chist. Un indicator important pentru corectitudinea celei de-a doua teorii a loviturilor sunt experimentele cu șoareci knockout în care PKD1 sau PKD2 au fost oprite ( ștergerea genei ). Doar animalele homozigote se îmbolnăvesc , în timp ce animalele heterozigote se dezvoltă aproape normal. A doua teorie a impactului explică, de asemenea, de ce doar aproximativ 1% din toate nefronele din ADPKD formează chisturi, chiar dacă toate celulele poartă mutația moștenită.
Începând cu 1995, o a treia genă, numită PKD3, a fost suspectată a fi o altă posibilă cauză a ADPKD. Mutațiile care nu au fost cauzate nici de PKD1, nici de PKD2 au fost observate ulterior în alte patru familii cu rinichi chistici din diferite țări. Existența acestei gene este acum pusă la îndoială.
| genă | Loci | Exoni | Tipul mutației | Frecvență (%) |
| PKD1 | 16p13.3 | 46 (14,1 kb) | Prostii | 33 |
| Frameshift | 28 | |||
| In rama | Al 6-lea | |||
| Împletirea | 14 | |||
| Missense | 19 | |||
| PKD2 | 4q21-q23 | 15 (5 kb) | Prostii | 37 |
| Frameshift | 39 | |||
| Împletirea | 17 | |||
| Missense | Al 6-lea | |||
| Ștergere | 1 |
Cauze moleculare și formarea chistului
Proteinele codificate de genele afectate polycystin-1 si polycystin 2 precum fibrocystin codificată de PKHD1 genei sunt situate la baza cilium primare a a celulelor tubilor renali (celule renale tubilor) . Ciliul primar este o extensie celulară subțire de păr, din care fiecare celulă dezvoltă doar una. Conform cunoștințelor actuale, o defecțiune a ciliului primar joacă rolul decisiv în formarea chisturilor în toate bolile care duc la rinichii chistului. Ciliile primare ale celulelor tubulare ies în lumenul tubular și probabil sunt folosite acolo pentru a percepe fluxul de fluid. În plus, ciliul primar este implicat în alinierea spațială a fusului mitotic în timpul diviziunii celulare . Cele două polycystines formează un calciu- regulator canal de ioni , care este permeabilă la ionii de calciu. Complexul de policistină joacă un rol important în ciliul primar cu mai multe căi de semnal și funcții mecanico-senzoriale. Funcția fiziologică a acestei organite celulare nu este încă în mare parte înțeleasă.
Originea chisturilor poate avea punctul de plecare în orice secțiune a nefronului - de la glomerul la canalele colectoare (tubulus renalis colligens) . Când chisturile ating un diametru mai mare de 0,2 mm, nu mai au nicio legătură cu tubii renali (tubuli) .
Pentru ca chisturile să se formeze, numărul de celule din peretele chistului trebuie să crească. Acest lucru se întâmplă prin proliferarea excesivă a celulelor epiteliale ale rinichilor. Proteina mTor (țintă de rapamicină la mamifere) este reglată în sus . De asemenea, lichidul trebuie să se acumuleze în lumenul chistului datorită secreției crescute și / sau scăderii drenajului. Această secreție de fluid transepitelial este dependentă de secreția de ioni clorură activă secundară. Secreția ionilor de clorură este reglementată de CFTR (regulator al conductanței transmembranare a fibrozei chistice) sau de un canal de clorură dependent de calciu. Ambele sunt situate în membrana celulară apicală .
Curs și prognostic
Cursul ADPKD este lent progresiv (progresiv). Chiar înainte de apariția insuficienței renale, la pacienții afectați poate fi detectată o perturbare a concentrației de urină (reabsorbția apei). În stadiile incipiente ale bolii, funcția renală nu este afectată de formarea chisturilor. Performanța scade doar de la o dimensiune a rinichilor de 1000 cm³. Dacă volumul rinichilor depășește 1500 cm³, rata de filtrare glomerulară este redusă anual cu aproximativ 4 până la 5 ml · min -1 . În medie, volumul rinichilor crește cu mai mult de 5% pe an la pacienții cu un volum renal mai mare de 750 cm³. Primele simptome ale bolii se observă de obicei între 30 și 40 de ani. Cu toate acestea, în general, există o gamă largă de variații - adesea în cadrul unei familii.
În aproape toate cazurile, boala duce la insuficiență renală terminală (insuficiență renală finală). Femeile ajung în această etapă în medie cu șase ani mai târziu decât bărbații.
Supraviețuirea suplimentară este apoi garantată numai prin terapia de substituție renală, adică dializă sau transplant de rinichi. Nu este încă pe deplin înțeles de ce rinichii polichistici duc în cele din urmă la stadiul final al bolii renale. Mecanismul nu poate fi explicat doar prin atrofia presiunii parenchimului. Intervențiile chirurgicale, cum ar fi puncțiile, nu întârzie evoluția bolii. Din examinările histologice se poate concluziona că hipertensiunea este un factor important pentru progresia (progresia) insuficienței renale.
În plus față de genetică, mediul și stilul de viață al pacientului au, de asemenea, un impact asupra evoluției ADPKD. La femei, de exemplu, s-a constatat că nașterile multiple și alți factori estrogeni înrăutățesc semnificativ evoluția bolii. Creșterea accelerată a chisturilor în comparație cu femeile și atingerea mai timpurie a insuficienței renale terminale la bărbați sunt, de asemenea, atribuite influențelor hormonale. De asemenea, fumatul de tutun influențează - în special în rândul bărbaților - progresia ADPKD negativă. O posibilă explicație este binecunoscutul efect negativ al fumatului asupra vaselor de sânge .
Speranța de viață
Într-un studiu, 333 de pacienți din 31 de familii cu PKD1 și 291 de pacienți cu PKD2 din 31 de familii au fost comparați cu un grup de control identic din punct de vedere geografic cu 398 de persoane. Pacienții cu PKD1 au atins o vârstă medie de 53,0 ani (± 1,8 ani; 95% probabilitate). Pe de altă parte, pacienții cu PKD2 au ajuns la o medie de 69,1 ani (± 2,2 ani; 95%), în timp ce persoanele din grupul de control aveau 78,0 ani (± 4,2 ani; 95%) (vezi graficul adiacent).
Cauzele morții
Cauza decesului a 129 de pacienți cu ADPKD a fost analizată într-un studiu retrospectiv. După aceea, 36% au murit de boli de inimă și 24% de infecții . În 94% dintre infecții, sepsisul (otrăvirea sângelui) a fost prezent. De autopsiile a relevat hipertrofie cardiacă , în 89% dintre toți pacienții și boala arterială coronariană în 81% . Un eveniment neurologic a dus la deces la 12% dintre pacienți și la o ruptură a anevrismului cerebral la 6%. Hemoragia cerebrală cauzată de hipertensiune a fost cauza decesului la 5% și un accident vascular cerebral ischemic la 1% dintre pacienți. Niciun pacient nu a murit de cancer la rinichi .
Boală renală polichistică autosomală recesivă
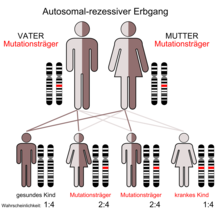
Boala renală polichistică autosomală recesivă ( ARPKD ), cunoscută și sub denumirea de rinichi burete sau rinichi Potter I , se manifestă în copilărie. Prevalența acestei boli la nou - nascuti este în intervalul de 1: 6000 până la 1: 40.000, cu o medie de 1: 20.000. Prin urmare, boala este relativ rară. Penetrance este completă. Aproximativ fiecare persoană a șaptezecea este un purtător al mutației (a se vedea diagrama moștenirii autozomale recesive). Mutațiile genei PKHD1 - care la om se află pe cromozomul 6 , locusul genei p21.1-p12 - poate duce la formarea rinichilor chistici. Proteina fibrocystin codificată de PKHD1 se găsește împreună cu -polycystin 2 în corpul bazal al cilia primare . În apicale domeniul celulelor epiteliale polarizate, este aparent implicat în formarea tubilor și / sau menținerea arhitecturii a lumenului tubului de colectare . În consecință, canalele colectoare sunt în esență afectate de formarea chistului în ARPKD. Boala renală polichistică autosomală recesivă este asociată cu fibroză hepatică congenitală.
ARPKD se manifestă la pacienți la o vârstă foarte fragedă ( debut precoce ) . Intervalul de vârstă este de la 0 la 20 de ani. Speranța medie de viață a copiilor afectați este de șase ani. Se face distincția între forma perinatală (a 28-a săptămână de sarcină până la șapte zile după naștere), neonatală (nou-născută), infantilă (infantilă) și juvenilă (adolescentă). Cu cât vârsta este mai mică la debut, cu atât prognosticul este mai rău .
Complex NPH-MCKD
Complexul NPH-MCKD (nefronoftiză-boală renală chistică medulară) este un grup de boli genetice ale rinichiului care duc la un rinichi chistic. În cazul nefronoftizei, moștenirea este autozomală recesivă, în timp ce este autosomală dominantă în ambele forme de boală renală chistică medulară. Tabloul clinic comun al bolilor este formarea rinichilor chistici la frontiera cortico-medulară (frontiera corticomedulară). În funcție de gena afectată, toate bolile complexului NPH-MCKD duc la insuficiență renală terminală în anumite intervale de vârstă.
Sindromul Bardet-Biedl
Sindromul Bardet-Biedl (BBS) este o boală ereditară oligogenetică foarte rară, cu o moștenire autozomală dominantă. Cauza bolii sunt mutatii ale genelor BBS 1 la 12. În plus față de formarea de rinichi polichistic, există degenerare retinei , copilarie obezitate , dizabilitatea intelectuală , malformații ale aparatului urinar și sexuale și polidactilie (mai multe degete) .
Scleroză tuberoasă
Chisturile renale individuale sunt frecvente în scleroza tuberoasă moștenită autozomal dominantă. Bolile renale polichistice sunt, de asemenea, mai puțin frecvente. Motivul pentru aceasta sunt de obicei deleții mai mari care afectează atât gena TSC2, care este afectată în scleroza tuberoasă, cât și gena PKD1; ambele gene sunt situate în imediata apropiere a cromozomului 16 .
Sindromul oro-facio-digital tip 1 (OFD 1)
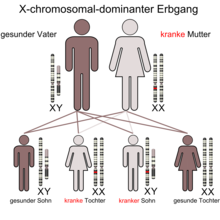
Sindromul oro-facio-digital de tip 1, cunoscut și sub numele de sindrom Papillon-Leage-Psaume, este o boală foarte rară , moștenită predominant, legată de X. Prevalența la nou-născuți este de aproximativ 1: 250.000. Boala are o serie de simptome diferite, în special ale feței și gurii, și o tendință de a prezenta rinichii polichistici la mulți pacienți. Acestea din urmă sunt diagnosticate de obicei foarte târziu când insuficiența renală este bine avansată.
Boala este fatală prenatal pentru bărbați .
Cu sindromul orofazio- digital tip 2 , OFD2 sau sindromul Mohr , nu se observă modificări ale rinichilor.
Rinichi chistic dobândit
O formă specială de Endstadiumniere, ca transformare secundară polichistică sau ca rinichi chistic dobândit (engl. Boala renală chistică dobândită , ACKD ) este menționată, la 50% din toți pacienții care se dezvoltă la 40 de ani după dializa pe termen lung. Ea este o complicație foarte gravă la ESRD ( boala renală în stadiul final al englezei , ESRD ). În cazul beneficiarilor de transplant , atât rinichii lor, cât și transplantul pot fi afectați. Cauza dezvoltării rinichilor chistului legat de dializă dobândită este de obicei o dializă pe termen lung pentru nefropatie analgezică . Chisturile la rinichi sunt foarte frecvente la pacienții cu boală renală în stadiu final. Frecvența și dimensiunea chisturilor cresc cu durata dializei. Ambele sexe sunt afectate în mod egal de boală, indiferent de vârsta pacientului. Probabilitatea ca cancerul de rinichi să se dezvolte ca o complicație suplimentară este semnificativ crescută - în special la pacienții de sex masculin.
terapie
În prezent, există un singur medicament aprobat pentru tratamentul bolilor renale polichistice ( tolvaptan , vezi mai jos). Aproximativ 50% din toți pacienții cu ADPKD - care reprezintă majoritatea pacienților cu afecțiuni renale polichistice - vor necesita terapie de substituție renală pe parcursul vieții. O vindecare este posibilă numai printr-un transplant de rinichi .
Măsuri adjuvante
Reglarea tensiunii arteriale, de obicei cu ajutorul inhibitorilor ECA , este de o importanță deosebită ca măsură adjuvantă în rinichii polichistici. În plus, există o serie de recomandări pentru pacienții cu rinichi chistici, care, de asemenea, nu permit o vindecare, dar fac progresul bolii mai favorabil pentru pacient.
Deoarece cofeina este suspectată că accelerează creșterea chistului, pacienții trebuie să evite băuturile care conțin cofeină, dacă este posibil. O dietă cu conținut scăzut de sare ajută la scăderea tensiunii arteriale, care este asociată cu excreția afectată a ionilor de sodiu. Medicamentele antiinflamatoare nesteroidiene , analgezicele mixte , anumite antibiotice și alte medicamente care sunt toxice pentru rinichi trebuie evitate pe cât posibil. Infecțiile chistice, pe de altă parte, sunt tratate cât mai devreme posibil cu antibiotice care pot penetra chistul sau bila .
Terapia de substituție renală
Doar terapia de substituție renală, adică dializa sau transplantul de rinichi, asigură supraviețuirea pacientului în insuficiență renală terminală. În majoritatea cazurilor, dializa se efectuează sub formă de hemodializă , deoarece rinichii supradimensionați - și adesea ficatul - fac cavitatea abdominală foarte înghesuită și, prin urmare, nu este posibilă dializa peritoneală . Dacă este posibil, transplantul de rinichi este de preferat dializei. Permite restabilirea performanței fizice, calității vieții și integrarea socială a pacientului. De asemenea, îmbunătățește semnificativ speranța de viață în comparație cu dializa. Timpii lungi de așteptare pentru rinichii donatorilor sunt problematici din cauza numărului redus de rinichi donatori disponibili.
Rinichii polichistici - spre deosebire de practica anterioară - sunt îndepărtați doar de pre-transplant în cazuri excepționale, de exemplu atunci când volumul de rinichi a atins o dimensiune critică.
Abordări terapeutice viitoare
Tratamentul pacienților cu rinichi chistic atrage costuri anuale de peste 1 miliard USD doar în SUA. Această sumă rezultă în esență din costurile pentru terapia de substituție renală necesare în insuficiența renală terminală.
Înmulțirea și creșterea dimensiunii chisturilor cu pereți subțiri, umplute cu lichid depind de două procese: proliferarea celulelor epiteliului chistului și secreția de lichid în chisturi. Ambele procese sunt dependente de AMPc . AMPc stimulează calea kinazei Ras / MAP și astfel duce la creșterea celulară anormală. În plus, AMPc activează canalul CFTR - clorură , promovând astfel secreția de lichid în chisturi. Abordările terapeutice testate în prezent se adresează atât proceselor dependente de AMPc, încât să încetinească formarea și creșterea chistului.
De asemenea, se efectuează cercetări privind posibila implicare a proteinei C-Met și, asociată cu aceasta, o terapie cu inhibitori de C-Met , care au arătat rezultate promițătoare în experimentele pe animale cu șoareci .
Proceduri de imagistică și investigarea noilor abordări terapeutice
Vârsta medie la diagnosticarea ADPKD este în prezent de 27 de ani. Dacă apare insuficiență renală, există o scădere rapidă a GFR de ± 5,9 ml / min pe an. Până în prezent, niciun studiu randomizat în această etapă târzie a bolii nu a putut demonstra efectul benefic al unui tratament. Datorită fazei presimptomatice îndelungate și a debutului tardiv al insuficienței renale , obiectivele primare care sunt de obicei examinate în studiile privind bolile renale cronice, cum ar fi timpul până la tratamentul dializei, dublarea creatininei serice sau decesul, sunt de utilizare limitată în studiile privind polichisticul. boală de rinichi. Din acest motiv a fost creat Consorțiul pentru Studii de Imagerie Radiologică a Bolilor Rinichilor Polichistice. (CRISP), a cărui sarcină este de a examina metodele imagistice care permit declarații despre evoluția bolii în stadiile incipiente. Un rezultat important al investigațiilor CRISP utilizând imagistica prin rezonanță magnetică este că chisturile la pacienții cu ACPKD cresc continuu și cuantificabile și că creșterea chistului se corelează cu scăderea funcției renale. Adică, o creștere mai mare a dimensiunii chistului este asociată cu o scădere mai rapidă a funcției rinichilor.
Boala renală polichistică HALT (HALT-PKD) este un studiu prospectiv care investighează în prezent efectele blocării sistemului renină-angiotensină-aldosteron și / sau a controlului strict al tensiunii arteriale în stadiile incipiente ale bolii asupra creșterii chistului sau în etapele ulterioare ale bolii afectează dublarea creatininei serice, debutul dializei și decesul.
Inhibarea proliferării celulare
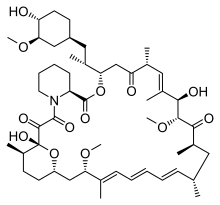
În ultimii ani, odată cu creșterea cunoștințelor biologice moleculare despre cauzele PKD, s-au găsit noi abordări terapeutice. Unele dintre aceste abordări sunt în prezent în testarea clinică . Inițial, însă, a fost mai mult o constatare incidentală: într-un studiu retrospectiv al unor pacienți cărora li s-a administrat un rinichi străin, s-a constatat că rinichiul polichistic rămas nu a crescut în volum, dar că unele chisturi s-au retras oarecum. Numărul pacienților din primul studiu (n = 4) nu a fost semnificativ statistic, dar efectul ar putea fi dovedit statistic în diferite modele animale . Cauza evidentă a acestei îmbunătățiri a fost administrarea de sirolimus (rapamicină), care a fost administrat pacienților ca medicament imunosupresor . Pacienții cu rinichi donator trebuie să ia imunosupresoare pentru întreaga lor viață, pentru a evita respingerea organului străin de către sistemul imunitar propriu al organismului . În studiile la om, tratamentul cu inhibitorii mTOR sirolimus și everolimus a încetinit creșterea volumului renal, dar nu și scăderea progresivă a funcției renale.
Pe lângă sirolimus și derivații acestui compus, se efectuează cercetări și asupra altor substanțe potențiale, dintre care unele utilizează alte căi de semnalizare. Astfel, de exemplu, cAMP - antagoniștii somatostatină și vasopresina potențial medicament deoarece nivelurile crescute de cAMP stimulează proliferarea și secreția celulelor epiteliale chistice.
Triptolida este o moleculă mică izolată dintr-un medicament tradițional chinezesc (Thunder God Vine) care are proprietăți anti-proliferative și pro- apoptotice . Triptolida favorizează eliberarea calciului printr-o cale metabolică dependentă de policistină-2 și inhibă formarea și creșterea chistului la modelele animale.
Inhibarea secreției de lichide
Nivelul hormonului antidiuretic (vasopresină) este crescut la pacienții cu boală renală polichistică . Receptorul de vasopresină V2 din tubul distal și canalul colector s-a exprimat . Acestea sunt locurile de pe nefron unde are loc formarea chistului. Vasopresina stimulează formarea AMPc în tubul distal prin receptorul V2.
În modelul animal, antagoniștii receptorilor V2 inhibă formarea AMPc, creșterea dimensiunii rinichilor și formarea chisturilor și protejează funcția renală.
Antagonistul receptorului V2 tolvaptan s-a dovedit a fi sigur și bine tolerat la pacienții cu ADPKD în studiile de fază II / III . Un studiu dublu-orb, controlat cu placebo, a fost efectuat la pacienții cu ADPKD, cu funcție renală normală și cu un volum renal mai mare de 750 ml. Tolvaptanul poate încetini progresia bolii. Tolvaptan a fost aprobat în Europa pentru tratamentul ADPKD din mai 2015.
Complicații
Complicațiile tipice ale rinichilor chistici sunt creșterea tensiunii arteriale datorită stimulării sistemului renină-angiotensină-aldosteron și a infecțiilor tractului urinar .
Infecțiile tractului urinar - datorate tractului urinar mai scurt - afectează în special pacienții de sex feminin. Cele mai multe cazuri sunt infecții ale vezicii urinare cauzate de gram-negative și nozocomiale germeni. Infecțiile tractului urinar sunt tratate simptomatic, de preferință cu antibiotice lipofile . Infecțiile extreme, cum ar fi pionefroza ( hidronefroza purulentă ), pot duce la îndepărtarea rinichiului afectat ( nefrectomie ).
În timp ce incidența calculilor renali în populație este de aproximativ 5%, aceste depozite afectează 10-34% dintre pacienții cu rinichi polichistic. O posibilă cauză a incidenței crescute a pietrelor la rinichi este nivelul scăzut al pH-ului în urină al celor afectați.
În funcție de autor și de studiul efectuat, 25 până la 75% din toți pacienții cu ADPKD cu rinichi chistici au și chisturi hepatice . Numărul de chisturi hepatice crește odată cu vârsta pacientului. Femeile au un număr mai mare și mai mare de chisturi pe ficat. Datorită chisturilor, ficatul poate fi mărit considerabil și literalmente pătruns cu chisturi. În majoritatea cazurilor, însă, funcția celulelor parenchimatoase nu este afectată. De exemplu, nivelul enzimelor hepatice și al bilirubinei sunt normale. Complicații mai extinse apar din necesarul de spațiu al ficatului uneori extrem de mărit. De exemplu, este posibil ca diafragma să fie ridicată , secțiuni individuale ale intestinului să fie îngustate, ceea ce poate îngreuna transportul alimentelor și vasele de sânge mai mari, cum ar fi vena cavă inferioară , pot fi obstrucționate .
ARPKD duce la fibroză, ciroză și presiune crescută în vena portă ( hipertensiune portală ) în ficat .
În alte organe, cum ar fi pancreasul , splina sau ovarele , chisturile sunt mult mai puțin frecvente la pacienții cu rinichi polichistic.
O conexiune între rinichii polichistici și anevrismele cerebrale a fost descrisă încă din 1904 . Datele privind prevalența variază între 4,5 și 22,5%. O posibilă ruptură (ruptură) a vasului de sânge afectat este una dintre cele mai temute complicații ale rinichilor chistici și este fatală în aproape 50% din cazuri.
istorie
Chirurgul parizian Félix Lejars (1863-1932) a folosit prima dată termenul de rinichi polichistic în disertație în 1888 . Canadian medic William Osler a descris -o în 1915. Până la mijlocul secolului 20, doar câteva publicații tratate cu acest tablou clinic. În disertația sa din 1957, Dalgaard a fost primul care a recunoscut moștenirea autosomală dominantă a ADPKD. În 1985, Reeders și colegii au descoperit locusul genei PKD1 pe cromozomul 16 la oameni.
literatură
Articol tehnic
- W. Kühn, G. Walz: Boli renale polichistice dominante autosomale. În: Dtsch Arztebl. , 104, 2007, pp. A3022-A3028.
- I. Ishikawa: Boală chistică renală dobândită. În: Rinichiul chistic. Kluwer, 1990, ISBN 0-7923-0392-X , pp. 351-377.
- JJ Grantham, PA Gabow: Boală renală polichistică. În: Boli ale rinichiului. Little Brown, 1988, pp. 583-615.
- Joachim Frey : rinichi chistici și alte anomalii congenitale. În: Ludwig Heilmeyer (ed.): Manual de medicină internă. Springer-Verlag, Berlin / Göttingen / Heidelberg 1955; Ediția a II-a, ibid. 1961, p. 974 f.
Carti de referinta
- ML Watson (Ed.): Boală renală polichistică. Oxford Univ. Presă, 1996, ISBN 0-19-262578-0 .
- HM Sass, P. Schröder (Ed.): Educația pacientului în cazul riscului genetic. LIT Verlag, 2003, ISBN 3-8258-4987-2 , pp. 147-198.
Informații despre pacienți
- AB Chapman, LM Guay-Woodford: Familia și ADPKD: un ghid pentru copii și părinți. Fundația de cercetare a rinichilor polichistici, 1997, ISBN 0-9614567-5-2 .
- Fișe de informații despre rinichii chistici într-un liant inelar . Asocierea pacientului PKDeV
Știința populară
- T. Kotlorz: Nouă speranță pentru pacienții cu rinichi. În: Die Welt , 23 iulie 2007
- H. Jänz: Sperăm în rinichi. În: Die Welt , 3 iunie 2006
Link-uri web
- Rinichi chistic familial PKD e. V.
- Manual de urologie: Boli renale polichistice dominante autosomale (ADPKD)
- zystennieren.de Universitatea Ruhr Bochum
- PathoPic - Baza de date de imagini a Universității din Basel: angiogramă postmortemă a unui rinichi chistic (imaginea unui specimen)
- PathoPic - Baza de date de imagini a Universității din Basel: ADPKD (Potter Type I) (imaginea unui specimen)
- PathoPic - Baza de date de imagini a Universității din Basel: rinichi polichistic după insuficiență renală terminală (imaginea unui preparat)
- PathoPic - Baza de date de imagini a Universității din Basel: ARPKD (Potter Type I) (imaginea unui specimen)
- PathoPic - Baza de date de imagini a Universității din Basel: doi rinichi polichistici și un rinichi de transplant (imaginea unui specimen)
Videoclipuri
- Profesorul Obermüller: Rinichii chistici sunt explicați clar - atacuri asupra unui organ performant de pe YouTube
- Rapoarte afectate pe YouTube
Dovezi individuale
- ^ S. Wang și colab.: Proteina bolii polichistice renale autozomale recesive este localizată în cilii primari, cu concentrație în zona bazală a corpului. În: J Am Soc Nephrol . , 15, 2004, pp. 592-602. PMID 14978161
- ↑ a b c d e f g h i j k l m n o p q r s t U. Faber: Curs pe termen lung de degenerescență renală polichistică la adulți după transplant renal. Disertație, Universitatea Heinrich Heine Düsseldorf, 2000.
- ^ J. Milutinovic și colab.: Boală renală polichistică autosomală dominantă: simptome și constatări clinice. În: QJ Med. , 53, 1984, pp. 511-522. PMID 6240069
- ^ LW Elzinga și colab.: Tratamentul chirurgical al rinichilor polichistici dureroși. În: Am J rinichi Dis . , 22, 1993, pp. 532-527. PMID 8213792
- ↑ LW Elzinga și colab.: Chirurgie în gestionarea bolii renale polichistice autosomale dominante. În: Am. J. Dis rinichi. , 1992, pp. 89-92. PMID 1739090
- ↑ D. Frang și colab.: O nouă abordare a tratamentului rinichilor polichistici. În: Int. Urol. Nefrol. , 20, 1988, pp. 13-21. PMID 3360583
- ↑ LW Elzinga și colab.: Chirurgie de decompresie a chistului pentru boala renală polichistică autosomală dominantă . În: J Am Soc Nephrol. , 2, 1992, pp. 1219-1226. PMID 1591362 .
- ↑ BJ Lifson u a.: Rolul și rezultatele pe termen lung ale decorticării laparoscopice în bolile renale polichistice chistice solitare și autosomale dominante. În: J Urol . , 159, 1998, pp. 702-705. PMID 9474129
- ↑ AB Chapman și colab.: Proteinuria și microalbuminuria obținute în bolile renale polichistice autosomale dominante. În: J Am Soc Nephrol. , 5, 1994, pp. 1349-1354. PMID 7894001
- ↑ PA Gabow și colab.: Structura renală și hipertensiunea arterială în boala renală polichistică autozomală dominantă. În: Kidney International , 38, 1990, pp. 1177-1180. PMID 2074659
- ↑ a b P. A. Gabow: Boală renală polichistică autosomală dominantă În: NEJM 329, 1993, pp. 332-342. PMID 8321262
- ^ AB Chapman, PA Gabow: Hipertensiune în boala renală polichistică autosomală dominantă. În: Kidney Int Suppl , 61, 1997, pp. 71-73. PMID 9328971
- ^ PA Gabow și colab.: Utilitatea ultrasonografiei în diagnosticul bolii renale polichistice dominante autozomale la copii. În: J Am Soc Nephrol. , 8, 1997, pp. 105-110. PMID 9013454
- ^ WC O'Neill și colab.: Evaluarea sonografică a severității și progresiei bolii renale polichistice autosomale dominante: Consorțiul de studii de imagistică renală în bolile renale polichistice (CRISP). În: Am J rinichi Dis. , 46, 2005, pp. 1058-1064. PMID 16310571
- ↑ KM Koch și colab.: Nefrologie clinică. Urban & Fischer-Verlag, 1999, ISBN 3-437-21730-5 , pp. 437-459.
- ↑ V. Osathanondh, EL Potter : Patogenia rinichilor polichistici. În: Arh. Calea. , 77, 1964, pp. 459-465. PMID 14120681
- ↑ B. Hermanns și colab.: Patologie și genetică a rinichilor chistici ereditari. În: Der Pathologe , 24, 2003, pp. 410-420. PMID 14605845
- ↑ ADPKD (Boli renale polichistice dominante autosomale) ( pagina nu mai este disponibilă , căutați în arhivele web ) Spitalul Universitar Aachen; Adus la 30 septembrie 2008.
- ↑ a b c S. Helmig: investigație genetică a populației asupra genei PKD 1 a pisicii în ceea ce privește sindromul polichistic. Disertație, Universitatea Justus Liebig Giessen, 2005.
- ↑ F. Hildebrandt, M. Wolf: Patologie și genetica rinichilor chistici ereditari. În: Terapie medicală. Springer, 2005, ISBN 3-540-21226-4 , pp. 927-939.
- ↑ a b c d e f g W. Kühn, G. Walz: Boală renală polichistică autosomală dominantă. În: Ärzteblatt , 104/2007, pp. A3022 - A3028.
- ^ RG Elles și colab.: Diagnosticul bolii renale polichistice la adulți prin markeri genetici și imagistică ultrasonografică într-un registru de familie voluntar. În: J Med Genet , 31, 1994, pp. 115-120. PMID 8182715 .
- ↑ LF Fried și colab.: Obstrucție duodenală în boala renală polichistică. Raport de caz și revizuirea literaturii. În: Am. J. Nefrol. , 18, 1998, pp. 318-320. PMID 9653836
- ↑ a b P.D. Wilson: boală renală polichistică. În: N Engl J Med. , 350, 2004, pp. 151-164. PMID 14711914 .
- ↑ U. Frei, HJ Schober-Halstenberg: Terapia de substituție renală în Germania. (PDF; 1,4 MB) În: Raportul anual QuaSi-Niere 2005/2006. Berlin
- ↑ GM Fick, PA Gabow: Boală chistică ereditară și dobândită a rinichiului. În: Rinichi Int. , 46, 1994, pp. 951-964. PMID 7861721 .
- ^ R. Rohatgi: Manifestări clinice ale bolii renale chistice ereditare. În: Front Biosci. , 13, 2008, pp. 4175-4197. PMID 18508505
- ↑ boală renală, chistic medular, autosomal dominant, cu sau fără hiperuricemie orfă.net; Adus la 4 octombrie 2008.
- ↑ M. Attanasio și colab.: Pierderea GLIS2 cauzează nefronoftiză la om și șoareci prin apoptoză crescută și fibroză. În: Nature Genet . , 39, 2007, pp. 1018-1024. PMID 17618285
- ↑ a b B. Buchholz: Interacțiunea funcțională a policistinei 2 și TRPV4. Disertație, Universitatea Albert Ludwig din Freiburg, 2004.
- ^ AR Gallagher și colab.: Baza moleculară a bolii renale polichistice autosomale dominante. În: Cellular and Molecular Life Sciences , 59, 2002, pp. 682-693. PMID 12022474 .
- ↑ ADPKD (Boli renale polichistice dominante autosomale) . ( Pagina nu mai este disponibilă , căutați în arhive web ) University Hospital Aachen; Adus la 11 noiembrie 2008.
- ^ DW Bianchi și colab.: Fetologie. McGraw-Hill Professional, 2000, ISBN 0-8385-2570-9 , p. 632.
- ↑ PA Gabow și colab.: Factori care afectează progresia bolii renale în boala renală polichistică autosomală dominantă. În: Rinichi Int. , 41, 1992, pp. 1311-1319. PMID 1614046
- ^ AC Ong, PC Harris: Patogeneza moleculară a ADPKD: complexul de policistină devine complex. În: Rinichi Int. , 67, 2005, pp. 1234-1247. PMID 15780076
- ^ S. Rossetti și colab.: Analiza mutației întregii gene PKD1: implicații genetice și diagnostice. În: Am. J. Hum. Genet. , 68, 2001, pp. 46-63. PMID 11115377
- ^ GG Germino: Boală renală polichistică autosomală dominantă: un model cu două lovituri. În: Hosp Pract. , 32, 1997, pp. 81-82, 85-88, 91-92. PMID 9078975
- ↑ Y. Pei și colab.: Mutațiile somatice PKD2 în chisturile individuale ale rinichilor și ficatului susțin un model de cistogeneză „cu două lovituri” în boala renală polichistică autosomală dominantă de tip 2. În: J Am Soc Nephrol. , 10, 1999, pp. 1524-1529. PMID 10405208
- ↑ F. Qian și colab.: Baza moleculară a formării chisturilor focale în bolile renale polichistice dominante autosomale umane de tip I. În: Cell , 87, 1996, pp. 979-987. PMID 8978603
- ↑ T. Watnick și colab.: Mutațiile PKD1 în chisturile ADPKD2 sugerează un efect patogen al mutațiilor trans-heterozigote. În: Nature Genetics , 25, 2000, pp. 143-144. PMID 10835625
- ↑ K. Hackmann: Investigații privind expresia genelor murine Pkd1 și Pkd2, genele ortologe ale bolii renale polichistice autosomale dominante (ADPKD). (PDF) Disertație, Universitatea Bielefeld, 2005.
- ↑ W. Lu și colab.: Debut tardiv al chisturilor renale și hepatice în heterozigoții vizați de Pkd1. În: Nature Genetics , 21, 1999, pp. 160-161. PMID 9988265
- ↑ G. Wu și colab.: Inactivarea somatică a Pkd2 are ca rezultat o boală renală polichistică. În: Cell , 93, 1998, pp. 177-188. PMID 9568711
- ↑ N. Bogdanova și colab.: Heterogenitatea genetică a bolii renale polichistice în Bulgaria. În: Hum Genet. , 95, 1995, pp. 645-650. PMID 7789949
- ↑ MC Daoust și colab.: Dovezi pentru un al treilea locus genetic pentru boala renală polichistică autosomală dominantă. În: Genomică , 25, 1995, pp. 733-736. PMID 7759112
- ^ AD Paterson, Y. Pei: Există o a treia genă pentru boala renală polichistică autosomală dominantă? În: Kidney International , 54, 1998, pp. 1759-1761. PMID 9844156
- ↑ M. Koptides, CC Deltas: Boală renală polichistică autosomală dominantă: genetică moleculară și patogenie moleculară. În: Hum Genet. , 107, 2000, pp. 115-126. PMID 11030408
- ↑ M. Consugar și colab.: PKD3 revizuit cu haplotipuri PKD1 și PKD2 îmbunătățite și screening pentru mutații. În: J Am Soc Nephrol. , 16, 2005, p. 358A.
- ^ AD Paterson, Y. Pei: PKD3-a fi sau a nu fi? În: Nephrol Dial Transplant , 14, 1999, pp 631-614. PMID 10570111
- ↑ Y. Pei și colab.: Boala bilineală și trans-heterozigoții în boala renală polichistică autosomală dominantă. În: Am J Hum Genet. , 68, 2001, pp. 355-363. PMID 11156533
- ^ A b S. Rosetti, PC Harris: corelații genotip-fenotip în bolile renale polichistice autosomale dominante și autosomale recesive. În: J Am Soc Nephrol. , 18, 2007, pp. 1374-1380. PMID 17429049
- ↑ a b C. Boucher, R. Sandford: boală renală polichistică autosomală dominantă (genele ADPKD, MIM 173900, gene PKD1 și PKD2, produse proteice cunoscute sub numele de policistină-1 și policistină-2). În: Eur J Hum Genet. , 12, 2004, pp. 347-354. PMID 14872199 .
- ↑ C. Stayner, J. Zhou: Canalele de policistină și bolile renale. În: Tendințe în științe farmacologice , 22, 2001, pp. 543-546. PMID 11698076
- ^ T. Watnick, G. Germino: De la cilii la chist. În: Nature Genetics , 34, 2003, pp. 355-356. PMID 12923538
- ^ BK Yoder: Rolul cililor primari în patogeneza bolii renale polichistice. În: J Am Soc Nephrol. , 18, 2007, pp. 1381-1388. PMID 17429051
- ↑ BK Yoder și colab.: Patogeneza moleculară a bolii renale polichistice dominante autozomale. În: Expert Rev Mol Med. , 17, 2006, pp. 1-22. PMID 16515728
- ↑ KD Gardner și colab.: De ce cresc chisturile renale. În: Am J Physiol. , 266, 1994, F353-359. PMID 8160782
- ↑ D. Rizk, AB Chapman: Boli renale chistice și moștenite. În: Am J rinichi Dis. , 42, 2003, pp. 1305-1317. PMID 14655206
- ↑ MHK Shokeir: Expresia bolii renale polichistice la adulți în copilărie: un studiu longitudinal. În: Clin. Genet. , 14, 1978, pp. 61-72. PMID 688689
- ↑ N. Gretz și colab.: Este genul un factor determinant pentru evoluția insuficienței renale? Un studiu asupra bolii renale polichistice autosomale dominante. În: Am J rinichi Dis. , 14, 1989, pp. 178-183. PMID 2672797 .
- ↑ R. Sherstha și colab.: Terapia cu estrogen postmenopauză stimulează selectiv extinderea hepatică la femeile cu boală renală polichistică dominantă autosomală. În: Hepatologie , 26, 1997, pp. 1282-1286. PMID 9362373 .
- ↑ PC Harris și colab.: Numărul de chisturi, dar nu și rata de creștere chistică este asociat cu gena mutantă în ADPKD. În: J Am Soc Nephrol. , 17, 2006, pp. 3013-3019. PMID 17035604
- ^ R. Magistroni și colab.: Corelația funcției genotipice în boala renală polichistică autosomală dominantă de tip 2. În: J Am Soc Nephrol. , 14, 2003, pp. 1164-1174. PMID
- ^ SR Orth și colab.: Fumatul ca factor de risc pentru insuficiența renală în stadiul final la bărbații cu boală renală primară. În: Rinichi Int. , 54, 1998, pp. 926-931. PMID 9734618
- ↑ SR Orth și colab.: Fumatul ca factor de risc pentru insuficiența renală în stadiul final la pacienții cu boală renală primară. În: Contrib Nephrol. , 130, 2000, pp. 109-123. PMID 10892557 .
- ↑ a b N. Hateboer: Comparația fenotipurilor bolilor renale polichistice tipurile 1 și 2. În: The Lancet , 353, 1999, pp 103-107. PMID 10023895
- ↑ GM Fick și colab.: Cauze de deces în boala renală polichistică autosomală dominantă. În: J Am Soc Nephrol. , 5, 1995, pp. 2048-2456. PMID 7579053
- ^ Boală renală polichistică autosomală recesivă (ARPKD), analiză completă a genelor. Clinica medicală Mayo; accesat pe 16 ianuarie 2018.
- ^ R. Witzgall: Noi dezvoltări în domeniul bolilor renale chistice. (PDF; 250 kB) În: Medicina moleculară curentă , 5, 2005, pp. 455-465. PMID 16101475 .
- ↑ K. Zerres și colab.: Boli renale polichistice recesive autozomale. În: J Mol Med. , 76, 1998, pp. 303-309. PMID 9587064
- ↑ ST Shaikewitz și colab.:. Boli renale polichistice recesive autozomale: probleme legate de variabilitatea prezentării clinice. În: J Am Soc Nephrol. , 3, 1993, pp. 1858-1862. PMID 8338916
- ↑ Capac EC: studii biologice moleculare asupra genei PKD1 la pisici. Disertație, Universitatea Justus Liebig Giessen, 2008.
- ↑ MZ Zhang și colab.: Proteina PKHD1 codificată de gena pentru boala renală polichistică autosomală recesivă se asociază cu corpuri bazale și cilii primari în celulele epiteliale renale. În: Proc Natl Acad Sci SUA , 101, 2004, pp. 2311-2316. PMID 14983006
- ↑ LM Guay-Woodford: boli renale chistice: diverse fenotipuri converg asupra complexului cilium / centrosom. În: Nefrologie pediatrică , 21, 2006, pp. 1369-1376. PMID 16823577
- ↑ T. Benzing și colab.: Semnalizarea Wnt în bolile renale polichistice . În: J Am Soc Nephrol. , 18, 2007, pp. 1389-1398. PMID 17429050
- ↑ SJ Ansley și colab.: Disfuncția corpului bazal este o cauză probabilă a sindromului pleiotrop Bardet-Biedl. În: Natura , 425, 2003, pp. 628-633. PMID 14520415
- ↑ Sampson și colab.: Boala chistică renală în scleroza tuberoasă: rolul genei bolii renale polichistice 1. În: Am J Hum Genet. , 1997 oct; 61 (4), pp. 843-851. PMID 9382094 .
- ↑ AA Connacher și colab.: Sindromul orofaciodigital de tip I asociat cu rinichii polichistici și agenezia corpului calos. În: J. Med. Genet. , 24, 1987, pp. 116-122. PMID 3560170
- ↑ SA Feather și colab.: Sindromul oral-facial-digital de tip 1 este o altă boală renală polichistică dominantă: caracteristicile clinice, radiologice și histopatologice ale unei noi rude. În: Nephrol Dial Transplant . , 12, 1997, pp. 1354-1361. PMID 9249769
- ^ E. Prati: sindromul Oro-facio-digital tip 1. (PDF) În: Orphanet Encyclopedia. Octombrie 2004.
- ↑ K. Zerres, S. Rudnik-Schöneborn: Boli renale polichistice. În: Manual de Medicină Moleculară. Springer-Verlag, Volumul 7 (Partea 2), 2000, pp. 281-295.
- ↑ a b M. A. Matson, EP Cohen: Boala renală chistică dobândită: apariție, prevalență și cancere renale. În: Medicine (Baltimore) , 69, 1990, pp. 217-226. PMID 2374506
- ^ W. Remmele: Pathologie 5. Springer, 1997, ISBN 3-540-61098-7 , p. 172.
- ^ Universitatea din Basel: rinichi chist secundar după dializă din cauza nefropatiei analgezice. Imagine a unui specimen histologic; Adus la 8 septembrie 2008.
- ↑ FA Belibi și colab.: Efectul cofeinei asupra celulelor epiteliale renale de la pacienții cu boală renală polichistică autozomală dominantă. În: J Am Soc Nephrol. , 13, 2002, pp. 2723-2729. PMID 12397042
- ↑ M. Schmid și colab.: Relația natriureză-presiune în boala renală polichistică. În: J. Hypertens. , 8, 1990, pp. 277-283. PMID 2159509
- ^ BZ Colleen: Boala renală polichistică: o prezentare generală și un comentariu. În: Dializă și transplant , 28, 1999, pp. 468-474.
- ↑ HH Knispel și colab.: Transplant în boală renală polichistică autozomală dominantă fără nefrectomie. În: Urol. Int. , 56, 1996, pp. 75-78. PMID 8659014
- ↑ Y. Pirson și colab.: Rezultatul terapiei de substituție renală în boala renală polichistică autozomală dominantă. În: Nephrol Dial Transplant. , 11, 1996, pp. 24-28. PMID 9044324
- ↑ JJ Grantham: Boală renală polichistică: boală veche într-un context nou. În: Trans Am Clin Climatol Conf. Univ. , 113, 2002, pp. 211-224. PMID 12053711
- ↑ JP Calvet: Strategii pentru a inhiba formarea chistului în ADPKD. În.: Clin J Am Soc Nephrol . , 2008; 3 (4), pp. 1205-1211. PMID 18434615
- ↑ S. Qin, M. Taglienti și colab.: Eșecul ubiquitinării c-Met duce la hiperactivarea semnalizării mTOR într-un model de șoarece de boală renală polichistică autosomală dominantă. În: Jurnalul de investigații clinice , volumul 120, numărul 10, octombrie 2010, pp. 3617-3628, doi: 10.1172 / JCI41531 , PMID 20852388 , PMC 2947217 (text complet gratuit).
- ↑ AB Chapman: Abordări pentru testarea noilor tratamente în bolile renale polichistice autozomale dominante: perspective din studiile CRISP și HALT-PKD. În: Clin J Am Soc Nephrol. , 3, 2008, pp. 1197-1204. PMID 18579674
- ↑ JJ Grantham și colab.: Progresia volumului în boala renală polichistică. În: NEJM , 354, 2006, pp. 2122-2230. PMID 16707749
- ↑ JM Shillingford și colab.: Calea mTOR este reglată de policistină-1 și inhibarea acesteia inversează cistogeneza renală în bolile renale polichistice. În: Proc Natl Acad Sci. , 103, 2006, pp. 5466-5471. PMID 16567633
- ↑ Y. Tao și colab.: Rapamicina încetinește semnificativ progresia bolii într-un model de șobolan de boală renală polichistică. În: J Am Soc Nephrol. , 16, 2005, pp. 46-51. PMID 15563559
- ↑ PR Wahl i.a .: Inhibarea mTOR cu sirolimus încetinește progresia bolii la șobolani Han: SPRD cu boală renală polichistică autosomală dominantă (ADPKD). În: Nephrol Dial Transplant. , 21, 2006, pp. 598-604. PMID 16221708 .
- ↑ SM Flechner și colab.: Transplantation , 74, 2002, pp. 1070-1076. PMID 12438948
- ↑ AL Serra, D. Poster, AD Kistler, F. Krauer, S. Raina, J. Young, KM Rentsch, KS Spanaus, O. Senn, P. Kristanto, H. Scheffel, D. Weishaupt, RP Wüthrich: Sirolimus și creșterea rinichilor în bolile renale polichistice autosomale dominante. În: The New England Journal of Medicine , volumul 363, numărul 9, august 2010, pp. 820-829, ISSN 1533-4406 . doi: 10.1056 / NEJMoa0907419 . PMID 20581391 .
- ↑ G. Walz, K. Budde, M. Mannaa, J. Nürnberger, C. Wanner, C. Sommerer, U. Kunzendorf, B. Banas, WH Hörl, N. Obermüller, W. Arns, H. Pavenstädt, J. Gaedeke, M. Büchert, C. May, H. Gschaidmeier, S. Kramer, KU Eckardt: Everolimus la pacienții cu boală renală polichistică autosomală dominantă. În: The New England Journal of Medicine , volumul 363, numărul 9, august 2010, pp. 830-840, ISSN 1533-4406 . doi: 10.1056 / NEJMoa1003491 . PMID 20581392 .
- ↑ a b A. Masoumi și colab.: Intervenții farmacologice potențiale în bolile renale polichistice. În: Droguri , 67, 2007, pp. 2495-2510. PMID 18034588
- ↑ FA Belibi și colab.: AMP ciclic promovează creșterea și secreția în celulele epiteliale renale polichistice umane. În: Rinichi Int. , 66, 2004, pp. 964-973. PMID 15327388
- ↑ T. Yamaguchi și colab.: AMPc stimulează proliferarea in vitro a celulelor epiteliale ale chistului renal prin activarea căii kinazei reglate de semnal extracelular. În: Rinichi Int. , 57, 2000, pp. 1460-1471. PMID 10760082
- ^ SJ Leuenroth și colab.: Triptolida reduce cistogeneza într-un model de ADPKD. În: J Am Soc Nephrol. , 19, 2008, pp. 1659-1662. PMID 18650476
- ↑ SJ Leuenroth și colab.: Triptolida este un inhibitor tradițional derivat din medicina chineză a bolii renale polichistice. În: Proc Natl Acad Sci. , 104, 2007, pp. 4389-4394. PMID 17360534
- ↑ a b V. E. Torres: Rolul antagoniștilor vasopresinei. În: Jurnalul Clinic al Societății Americane de Nefrologie , Volumul 3, Numărul 4, iulie 2008, pp. 1212-1218. doi: 10.2215 / CJN.05281107 . PMID 18434616 . (Revizuire).
- ^ VE Torres și colab.: Tratamentul eficient al unui model ortolog al bolii renale polichistice dominante autozomale. În: Nat Med , 10, 2004, pp. 363-364. PMID 14991049 .
- ↑ Studiu clinic (faza III): "TEMPO 3/4 Trial" Tolvaptan Eficacitate și siguranță în gestionarea bolii renale polichistice și a rezultatelor sale (TEMPO3 / 4) la Clinicaltrials.gov al NIH
- ↑ V. Patel, R. Chowdhury, P. Igarashi: Progrese în patogeneza și tratamentul bolilor renale polichistice. În: Opinia curentă în Nefrologie și hipertensiune, volumul 18, numărul 2, martie 2009, pp. 99-106, ISSN 1535-3842 . doi: 10.1097 / MNH.0b013e3283262ab0 . PMID 19430332 . PMC 282027 (text complet gratuit). (Revizuire).
- ^ VE Torres: antagoniști ai vasopresinei în bolile renale polichistice. În: Seminarii în Nefrologie , 2008, 28, pp. 306-317. doi: 10.1016 / j.semnephrol.2008.03.003 . PMID 18519091 . (Revizuire).
- ↑ VE Torres și colab.: Boala de calculi renali în boala renală polichistică autosomală dominantă. În: Am. J. Dis rinichi. , 22, 1993, pp. 513-519. PMID 8213789
- ↑ J. Milutinovic și colab.: Chisturi hepatice la pacienții cu boală renală polichistică autozomală dominantă. În: Am. J. Med. , 68, 1980, pp. 741-744. PMID 7377224
- ↑ a b E. Higashihara și colab.: Aspecte clinice ale bolii renale polichistice. În: J. Urol. , 147, 1992, pp. 329-332. PMID 1732586 .
- ^ Y. Itai și colab.: Chisturi hepatobiliare la pacienții cu boală renală polichistică autosomală dominantă: prevalență și constatări CT. În: Am. J. Roentgenol. , 164, 1995, pp. 339-342. PMID 7839965
- ↑ PA Gabow și colab.: Factori de risc pentru dezvoltarea chisturilor hepatice în boala renală polichistică autosomală dominantă. În: Hepatologie , 11, 1990, pp. 1033-1037. PMID 2365280
- ^ E. Levine și colab.: Chisturi hepatice în boala renală polichistică autosomală dominantă: studiu clinic și tomografic computerizat. (PDF) În: Am. J. Roentgenol. , 145, 1985, pp. 229-233. PMID 3875218
- ↑ A. Telenti și colab.: Infecția cu chist hepatic în boala renală polichistică autosomală dominantă. În: Mayo Clin. Proc. , 65, 1990, pp. 933-942. PMID 2198396
- ↑ WI Schievink și colab.: Anevrisme intracraniene saculare în bolile renale polichistice dominante autosomale. În: J. Am. Soc. Nefrol. 3, 1992, pp. 88-95. PMID 1391712 .
- ↑ AB Chapman și colab.: Anevrisme intracraniene în boala renală polichistică dominantă autosomală. În: NEJM , 327, 1992, pp. 916-920. PMID 1513348
- ↑ F. Lejars: You gros reins polykystique de l'adult. Disertație, 1888, Paris
- ↑ B. Schulze: rinichi chistici: pe drumul către o boală tratabilă. (PDF) În: MedReport , 44, 2006, p. 5.
- ^ W. Osler: Diagnosticul rinichiului polichistic. În: Internat Clin. , Philadelphia, 2, 1915, pp. 1-5.
- ^ LP Brendan și colab.: A făcut Sir William Osler o autopsie la spitalul Johns Hopkins? În: Archives of Pathology & Laboratory Medicine , 2, 132, 2007, pp. 261-264.
- ^ OZ Dalgaard: Boală polichistică bilaterală a rinichilor. În: Acta Med Scand. , 328, 1957, pp. 1-255. PMID 13469269
- ^ ST Reeders și colab.: Un marker ADN extrem de polimorf legat de boala renală polichistică adultă pe cromozomul 16. În: Nature , 317, 1985, pp. 542-544. PMID 2995836